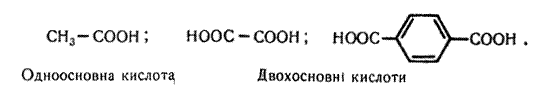194. Хімія
4. Оксигеновмiснi органiчнi сполуки
Автор: Бубенщикова Г.Т.
| • 1 |
| Текст к ситуации | ЛАБОРАТОРНА РОБОТА № 4 "ОКСИГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ" ЗАГАЛЬНІ ВКАЗІВКИ Виконання лабораторної роботи починається з уважного опрацювання теоретичного матеріалу теми, короткий зміст якого наведено перед завданнями до роботи. Не познайомившись з цим матеріалом, студент не зможе вірно осмислити суть хімічного експерименту, описати його та зробити висновки. Тому перед безпосереднім виконанням роботи студент повинен відповісти на ряд запитань, які мають за мету перевірити ступінь засвоєння теми, і при достатньому рівні засвоєння одержати дозвіл на виконання роботи. Після того, як всі досліди лабораторної роботи будуть виконані, зафіксовані і осмислені, студент повинен оформити журнал проведення дослідів, форму якого наведено нижче. Оформлений лабораторний журнал (звіт-таблиця) надсилається викладачу, який перевіряє його, робить зауваження, і зараховує (або не зараховує) лабораторну роботу, про що повідомляє студента. В даній лабораторній роботі треба обов’язково назвати продукти реакцій!!! Без назв речовин робота не буде зарахована викладачем. |
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 2 |
| Текст к ситуации | Уважного опрацюйте теоретичний матеріал теми. Не познайомившись з цим матеріалом, ви не зможете вірно осмислити суть хімічного експерименту, описати його та зробити висновки. |
| 1 | Продовжити виконання лабораторної роботи | 3 |
| 2 | СПИРТИ, ФЕНОЛИ | 101 |
| 3 | КАРБОНІЛЬНІ СПОЛУКИ | 102 |
| 4 | КАРБОНОВІ КИСЛОТИ | 103 |
| • 3 |
| Текст к ситуации | УВАГА! Для виконання лабораторної роботи Вам треба відповісти на декілька запитань у вигляді тестування. Допуск на виконання лабораторної роботи Ви одержуєте тільки після вірних відповідей.
Далі Вам буде запропоновано 4 питання по темі «Оксигеновмісні органічні сполуки (спирти, альдегіди, кетони, карбонові кислоти». У разі невірної відповіді хоч на одне питання результат не зараховується і Ви повертаєтесь на початок тестування. |
| 1 | Почати тестування | 5, 6, 7 |
| • 4 |
| Текст к ситуации | Помилка тесту.
На жаль, Ви неправильно відповіли на питання тесту, тому пропонуємо Вам уважно перег-лянути теоретичний матеріал і після цього спробувати повторно надати відповіді на питан-ня тестового контролю. |
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 5 |
| Ограничение времени | 5 минут |
| Текст к ситуации | При окисненні первинних спиртів утворюються: |
| 1 | кетони | 4 |
| 2 | вторинні спирти | 4 |
| 3 | альдегіди | 8, 9, 10 |
| • 6 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Спирти одержують з алкенів реакцією: |
| 1 | гідратації | 8, 9, 10 |
| 2 | гідрування | 4 |
| 3 | дегідратації | 4 |
| • 7 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Реакція взаємодії спиртів з карбоновими кислотами називається: |
| 1 | карбоксилювання | 4 |
| 2 | дегідратації | 4 |
| 3 | естеріфікації | 8, 9, 10 |
| • 8 |
| Ограничение времени | 5 минут |
| Текст к ситуации | В реакції міжмолекулярної дегідратації спиртів утворюються: |
| 1 | естери | 4 |
| 2 | етери | 11, 12, 13 |
| 3 | алкени | 4 |
| 4 | двохатомні спирти | 4 |
| • 9 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Якісна реакція на багатоатомні спирти – це реакція взаємодії з: |
| 1 | аміачним розчином арґентум (І) оксиду | 4 |
| 2 | свіже осадженим купрум (ІІ) гідроксидом | 11, 12, 13 |
| 3 | бромною водою | 4 |
| 4 | розчином калій перманганату | 4 |
| • 10 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Гліцерин (гліцерол) належить до класу: |
| 1 | Одноатомних спиртів | 4 |
| 2 | двохатомних спиртів | 4 |
| 3 | трикарбонових кислот | 4 |
| 4 | трьохатомних спиртів | 11, 12, 13 |
| • 11 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Альдегіди можна одержати реакцією |
| 1 | відновлення первинних спиртів | 4 |
| 2 | окиснення первинних спиртів | 14, 15, 16 |
| 3 | окиснення вторинних спиртів | 4 |
| • 12 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Для якісного визначення альдегідів використовують реакцію: |
| 1 | взаємодії з купрум (ІІ) гідроксидом при нагріванні | 14, 15, 16 |
| 2 | відновлення воднем в присутності каталізатора | 4 |
| 3 | альдольної конденсації | 4 |
| • 13 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Формалін - це |
| 1 | 30-40%-ний водний розчин оцтового альдегіда | 4 |
| 2 | 30-40%-ний водний розчин мурашиного альдегіда | 14, 15, 16 |
| 3 | 30-40%-ний спиртовий розчин ацетону | 4 |
| • 14 |
| Ограничение времени | 5 минут |
| Текст к ситуации | З ростом молекулярної маси розчиність карбонових кислот у воді: |
| 1 | зменшується | 17 |
| 2 | збільшується | 4 |
| 3 | практично не змінюється | 4 |
| • 15 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Вкажіть формулу та тип олеїнової кислоти: |
| 1 | C17H35COOH; вища насичена карбонова кислота | 4 |
| 2 | C17H35COOH; вища ненасичена карбонова кислота | 4 |
| 3 | C17H33COOH; вища ненасичена карбонова кислота | 17 |
| • 16 |
| Ограничение времени | 5 минут |
| Текст к ситуации | При взаємодії пропанової кислоти з 2-пропанолом в присутності концентрованої сульфатної кислоти при нагріванні утворюється: |
| 1 | ізопропілацетат | 4 |
| 2 | пропіловий естер пропанової кислоти | 4 |
| 3 | ізопропілпропаноат | 17 |
| • 17 |
| Текст к ситуации | Ви успішно завершили тестування.
Можна приступити до виконання лабораторної роботи № 4 "ОКСИГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ". |
| 1 | Продовжити виконання лабораторної роботи | 18 |
| • 18 |
| Текст к ситуации | Лабораторна робота № 4 "ОКСИГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ" Звіт лабораторної роботи заповнюється у формі таблиці після виконання лабораторної роботи або після виконання кожного досліду. Ми рекомендуємо заповняти таблицю звіту після виконання кожного досліду! Починайте виконувати досліди. Бажаємо успіху!
ЛАБОРАТОРНА РОБОТА №4 "Оксигеновмісні органічні исполуки" (назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід 1. Утворення алкоголятів натрію і їх гідроліз
Спостереження:
Спостереження: Висновок: Дослід 2. Утворення купрум (ІІ) гліцерату
Спостереження: Висновок: Дослід 3. Окиснення спиртів купрум (ІІ) оксидом
Спостереження: Висновок: Дослід 4. Реакція “срібного дзеркала” на альдегіди
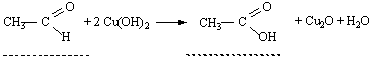
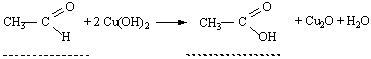
Спостереження: Висновок: Дослід 5. Взаємодія альдегідів з купрум (ІІ) гідроксидом
Спостереження: Висновок: Дослід 6. Взаємодія карбонових кислот з металами
Спостереження: Висновок: Дослід 7. Властивості ненасичених карбонових кислот
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 20 |
| • 19 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 20 |
| • 20 |
| Иллюстрация к шагу | 0194-04-020.mp4 |
| Текст к ситуации | Дослід 1. Утворення та гідроліз алкоголятів натрію Хід виконання досліду. В пробірку налити 2 мл етанола, додати шматочок очищеного металічного натрію, попередньо висушеного між аркушами фільтрувального паперу від гасу.. Що при цьому спостерігається? Після повного розчинення натрію у пробірку додати 2…3 мл води і 1…2 каплі фенолфталеїну. Уважно продивіться схему досліду та відеофрагмент його виконання, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції втаблицю звіту виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 21 |
| • 21 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Охарактеризуйте реакцію взаємодії етилового спирту з металічним натрієм: |
| 1 | 2 C2H5OH + 2 Na = 2 C2H5ONa + H2 Виділяється газ водень, який згоряє яскравим полум’ям | 19 |
| 2 | 2 C2H5OH + 2 Na = 2 C2H5ONa + H2 Виділяється газ водень, який згоряє з хлопком | 22 |
| 3 | 2 CН3OH + 2 Na = 2 CН3ONa + H2 Виділяється газ водень, який згоряє з хлопком | 19 |
| • 22 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Охарактеризуйте реакцію гідролізу продукту взаємодії етанолу з натрієм - натрій етилату, поясніть зміну забарвлення індикатора: |
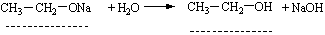
| 1 | C2H5ONa + H2O = C2H5OH + NaOH Забарвлення фенолфталеїна стає малиновим, оскільки внаслідок гідролізу утворюється луг. | 23 |
| 2 | C2H5ONa + H2O = C2H5OH + NaOH Забарвлення фенолфталеїна залишається безбарвним, оскільки внаслідок гідролізу утворюється спирт. | 19 |
| 3 | CН3ONa + H2O = CН3OH + NaOH Забарвлення фенолфталеїна стає малиновим, оскільки внаслідок гідролізу утворюється спирт. | 19 |
| • 23 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 1.
Рекомендуємо занести результати спостереження та рівняння реакцій у таблицю звіту виконання лабораторної роботи. Обов’язково назвіть продукти реакції. Далі можна приступити до виконання Досліду 2.
ЛАБОРАТОРНА РОБОТА №4 "Оксигеновмісні органічні исполуки" (назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід 1. Утворення алкоголятів натрію і їх гідроліз
Спостереження:
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 25 |
| • 24 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 25 |
| • 25 |
| Иллюстрация к шагу | 0194-04-025.mp4 |
| Текст к ситуации | Дослід 2. Утворення купрум (ІІ) гліцерату
Хід виконання досліду. В пробірку налити 2 мл розчину натрій гідроксиду, стільки же роз-чину купрум (ІІ) сульфату, 1 мл гліцерилу і збовтати. Уважно продивіться схему досліду та відеофрагмент його виконання, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції в таблицю звіту виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 26 |
| • 26 |
| Ограничение времени | 10 минут |
| Иллюстрация к шагу | 0194-04-026-00.gif |
| Текст к ситуации | З ілюстрації до даного досліду виберіть правильне рівняння реакції взаємодії гліцеролу з свіже осадженим купрум (ІІ) гідроксидом |
| 1 | Варіант 1 | 27 |
| 2 | Варіант 2 | 24 |
| 3 | Варіант 3 | 24 |
| • 27 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Виберіть рівняння одержання свіже осадженого купрум (ІІ) гідроксиду, охарактеризуйте його агрегатний стан, колір, та зміни, що відбуваються з ним при взаємодії з гліцеролом |
| 1 | Cu2SO4 + 2 NaOH = Na2SO4 + 2 CuOH CuOH - осад блакитного кольору; при взаємодії з гліцеролом розчиняється з утворенням синього розчину купрум (ІІ) гліцерату | 24 |
| 2 | CuSO4 + 2 NaOH = Na2SO4 + Cu(OH)2 Cu(OH)2 - осад блакитного кольору; при взаємодії з гліцеролом розчиняється з утворенням синього розчину купрум (ІІ) гліцерату | 28 |
| 3 | CuSO4 + 2 NaOH = Na2SO4 + Cu(OH)2 Cu(OH)2 - осад блакитного кольору; при взаємодії з гліцеролом перетворюється на осад синього кольору – купрум ( ІІ) гліцерат | 24 |
| • 28 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 2
Рекомендуємо занести результати спостереження та рівняння реакцій у таблицю звіту виконання лабораторної роботи. Обов’язково назвіть продукти реакції. Далі можна приступити до виконання Досліду 3.
(назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід2. Утворення купрум (ІІ) гліцерату
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 30 |
| • 29 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 30 |
| • 30 |
| Иллюстрация к шагу | 0194-04-030.mp4 |
| Текст к ситуации | Дослід 3. Окиснення спиртів купрум (ІІ) оксидом Хід виконання досліду. В пробірку налити 3…4 мл етанолу. Спіраль з мідної дротинки внести в полум’я пальника і нагріти до червоного жару. При цьому мідь окиснюється до купрум (ІІ) оксиду (чорного кольору). Розпечену окиснену спіраль занурити в пробірку з спиртом. Цю операцію повторити 3 рази. Після охолодження пробірки додати декілька крапель фуксинсульфітної кислоти. Уважно продивіться схему досліду та відеофрагмент його виконання, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції в таблицю звіту виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 31 |
| • 31 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Які зміни відбуваються на поверхні мідної спіралі після занурення у спирт? Чому? Виберіть рівняння реакції взаємодії етанолу з купрум (ІІ) оксидом. |
| 1 | Утворюється мідь червоного кольору внаслідок окиснення купрум (ІІ) оксиду. Спирт відновлюється до кислоти: CuO + C2H5OH = CH3COOH + Cu | 29 |
| 2 | Утворюється мідь червоного кольору внаслідок відновлення купрум (ІІ) оксиду. Спирт окиснюється до кетону: Cu2O + C2H5OH = CH3COH + 2Cu + H2O | 29 |
| 3 | Утворюється мідь червоного кольору внаслідок відновлення купрум (ІІ) оксиду. Спирт окиснюється до альдегіду: CuO + C2H5OH = CH3COH + Cu + H2O | 32 |
| • 32 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Як і чому змінює забарвлення фуксинсульфітна кислота? |
| 1 | Фуксинсульфітна кислота (безбарвна) змінює забарвлення на рожево-червоне, така зміна відбувається в присутності альдегідної групи (якісна реакція на альдегідну групу) | 33 |
| 2 | Фуксинсульфітна кислота (безбарвна) змінює забарвлення на синє, така зміна відбувається в присутності карбоксильної групи (якісна реакція на карбоксильну групу) | 29 |
| 3 | Фуксинсульфітна кислота залишається безбарвною, оскільки утворився кетон | 29 |
| • 33 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 3.
Рекомендуємо занести результати спостереження та рівняння реакцій у таблицю звіту виконання лабораторної роботи. Обов’язково назвіть продукти реакції. Далі можна приступити до виконання Досліду 4.
(назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід 3. Окиснення спиртів купрум (ІІ) оксидом
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 35 |
| • 34 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 35 |
| • 35 |
| Иллюстрация к шагу | 0194-04-035.mp4 |
| Текст к ситуации | Дослід 4. Реакція «срібного дзеркала» на альдегіди Хід виконання досліду. В чисту пробірку налити 3…4 мл 1 %-ного розчину арґентум (І) нітрату і додати краплями 5 %-ний розчин амоніаку в такій кількості, щоб осад, що спочат-ку утворився, повністю розчинився. До одержаного аміачного розчину арґентум (І) оксиду додати 1 мл мурашиного альдегіду і обережно нагріти на водяній бані за температури 60…70оС. Уважно продивіться схему досліду та відеофрагмент його виконання, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції в таблицю звіту виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 36 |
| • 36 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Реакції утворення аміачного розчину аргентум (І) оксиду |
| 1 | AgNO3 + NH3•H2O = AgO + NH4NO3 + Н2О Білий осад AgO при подальшому додавані розчину амоніаку розчиняється з утворенням комплексної сполуки: AgO + 2 NH3•H2O = 2 [Ag(NH3)2](OH)2 | 34 |
| 2 | 2 AgNO3 + 2 NH3•H2O = Ag2O + 2 NH4NO3 + 2 Н2О Бурий осад Ag2O при подальшому додавані розчину амоніаку розчиняється з утворенням сріблястої сполуки: Ag2O + 2 NH3•H2O = 2 Ag(NH3)2]OH | 34 |
| 3 | 2 AgNO3 + 2 NH3•H2O = Ag2O + 2 NH4NO3 + 2 Н2О Білий осад Ag2O при подальшому додавані розчину амоніаку розчиняється з утворенням комплексної сполуки: Ag2O + 2 NH3•H2O = 2 [Ag(NH3)2]OH | 37 |
| • 37 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Рівняння реакції утворення «срібного дзеркала» при взаємодії мурашиного альдегіда з аміачним розчином аргентум (І) оксиду: |
| 1 | CH3COH + 2[Ag(NH3)2]OH = CH3COOH +2Ag + 4 NH3 + H2O | 34 |
| 2 | HCOH + 2[Ag(NH3)2]OH = HCOOH +2Ag + 4 NH3 + H2O | 38 |
| 3 | HCOH + 2[Ag(NH3)2]OH = CH3OH +2Ag + 4 NH3 + H2O | 34 |
| • 38 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 4.
Рекомендуємо занести результати спостереження та рівняння реакцій у таблицю звіту виконання лабораторної роботи. Обов’язково назвіть продукти реакції. Далі можна приступити до виконання Досліду 5.
(назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід 4. Реакція “срібного дзеркала” на альдегіди
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 40 |
| • 39 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 40 |
| • 40 |
| Иллюстрация к шагу | 0194-04-040.mp4 |
| Текст к ситуации | Дослід 5. Взаємодія альдегідів з купрум (ІІ) гідроксидом Хід виконання досліду. У пробірку налити 1 мл оцтового альдегіду, 4 мл 10 %-ного розчи-ну натрій гідроксиду і додати краплями 2 %-ний розчин купрум (ІІ) сульфату до появи оса-ду. Обережно нагріти верхню частину вмісту пробірки. Уважно продивіться схему досліду та відеофрагмент його виконання, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції в таблицю звіту виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 41 |
| • 41 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Якого кольору осад спочатку утворюється в пробірці і за яким рівнянням: |
| 1 | Білий осад Cu(OH)2 : Сu2SO4 + 2 NaOH = 2 Cu(OH)2 + Na2SO4 | 39 |
| 2 | Блакитний осад Cu(OH)2 : СuSO4 + 2 NaOH = 2 Cu(OH)2 + Na2SO4 | 42 |
| 3 | Блакитний осад CuOH : Сu2SO4 + 2 NaOH = 2 CuOH + Na2SO4 | 39 |
| • 42 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Виберіть правильне рівняння реакції взаємодії оцтового альдегіду з купрум (ІІ) гідроксидом при нагріванні. Який осад і якого кольору утворюється? |
| 1 | CH3COH + 2СuOH = CH3COOH +2Cu + H2O Cu – червоного кольору | 39 |
| 2 | HCOH + 2Сu(OH)2 = HCOOH + Cu2O + H2O Cu2O – цегляно-червоного кольору | 39 |
| 3 | CH3COH + 2Сu(OH)2 = CH3COOH + Cu2O + H2O Cu2O - цегляно-червоного кольору | 43 |
| • 43 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 5.
Рекомендуємо занести результати спостереження та рівняння реакцій у таблицю звіту виконання лабораторної роботи. Обов’язково назвіть продукти реакції. Далі можна приступити до виконання Досліду 6.
(назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід 5. Взаємодія альдегідів з купрум (ІІ) гідроксидом
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 45 |
| • 44 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 45 |
| • 45 |
| Иллюстрация к шагу | 0194-04-045.mp4 |
| Текст к ситуации | Дослід 6. Взаємодія карбонових кислот з металами
Хід виконання досліду. У дві пробірки налити по 2 мл 50 %-ної оцтової кислоти. В одну по-класти стружку (або порошок) магнію, в іншу – шматочок цинку. Якщо реакція відбуваєть-ся повільно нагріти пробірку. Уважно продивіться схему досліду та відеофрагмент його виконання, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції в таблицю звіту виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 46 |
| • 46 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Як взаємодіє оцтова кислота з магнієм? |
| 1 | Виділяється безбарвний газ водень, реакція перебігає повільніше, ніж реакція цинка з оцтовою кислотою. СH3COOH + Mg = CH3COOMg + H2 | 44 |
| 2 | Виділяється безбарвний газ водень, реакція перебігає швидше, ніж реакція цинка з оцтовою кислотою. СH3COOH + Mg = CH3COOMg + H2 | 44 |
| 3 | Виділяється безбарвний газ водень, реакція перебігає швидше, ніж реакція цинка з оцтовою кислотою. 2 СH3COOH + Mg = (CH3COO)2Mg + H2 | 47 |
| • 47 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Як взаємодіє оцтова кислота з цинком? |
| 1 | Виділяється безбарвний газ водень, реакція перебігає повільніше, ніж реакція магнію з оцтовою кислотою. СH3COOH + Zn = CH3COOZn + H2 | 44 |
| 2 | Виділяється безбарвний газ водень, реакція перебігає повільніше, ніж реакція магнію з оцтовою кислотою. 2 СH3COOH + Zn = (CH3COO)2Zn + H2 (при нагріванні) | 48 |
| 3 | Виділяється безбарвний газ кисень, реакція перебігає швидше, ніж реакція магнію з оцтовою кислотою. 2 СH3COOH + Zn = (CH3COO)2Zn + H2 | 44 |
| • 48 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 6.
Рекомендуємо занести результати спостереження та рівняння реакцій у таблицю звіту виконання лабораторної роботи. Обов’язково назвіть продукти реакції. Далі можна приступити до виконання Досліду 7. (назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід 6. Взаємодія карбонових кислот з металами
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 50 |
| • 49 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 50 |
| • 50 |
| Иллюстрация к шагу | 0194-04-050.mp4 |
| Текст к ситуации | Дослід 7. Взаємодія олеїнової кислоти з бромом
Хід виконання досліду. У пробірку налити 2 мл олеїнової кислоти, додати 4…5 мл бромної води і сильно струсити. Уважно продивіться схему досліду та відеофрагмент його виконання, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції в таблицю звіту виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 51 |
| • 51 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Які зміни відбуваються у пробірці (зміна звбарвлення, утворення малорозчинних сполук)? |
| 1 | Бромна вода знебарвлюється. Утворюється білий розчин дибромолеїнової кислоти. | 49 |
| 2 | Бромна вода знебарвлюється. Утворюється білий осад дибромстеаринової кислоти. | 52 |
| 3 | Бромна вода стає білою. Утворюється безбарвний розчин дибромолеїнової кислоти. | 49 |
| • 52 |
| Ограничение времени | 10 минут |
| Текст к ситуации | Виберіть правильне рівняння реакції взаємодії олеїнової кислоти з бромомі. Вкажіть особливості будови олеїнової кислоти, завдяки яким ця реакція можлива: |
| 1 | C17H35COOH + Br2 = C17H33Br2COOH + Н2 Олеїнова кислота містить один подвійний зв’язок | 49 |
| 2 | C17H33COOH + Br2 = C17H35Br2COOH Олеїнова кислота містить один подвійний зв’язок | 53 |
| 3 | C17H33COOH + Br2 = C17H35Br2COOH Олеїнова кислота містить два подвійних зв’язка. | 49 |
| • 53 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 7.
Рекомендуємо занести результати спостереження та рівняння реакцій у таблицю звіту виконання лабораторної роботи. Обов’язково назвіть продукти реакції.
(назвати речовини, що підкреслено, записати спостереження і зробити висновки!!!!!!) Дослід 7. Властивості ненасичених карбонових кислот
Спостереження: Висновок: |
| 1 | Продовжити виконання лабораторної роботи | 54 |
| • 54 |
| Текст к ситуации | ВІТАЄМО ВАС! Ви успішно закінчили лабораторну роботу № 4 Перевірте правильність заповнення звіту виконання лабораторної роботи № 4 та надішліть його викладачу для перевірки (на адресу деканату заочного дистанційного навчання) |
| • 101 |
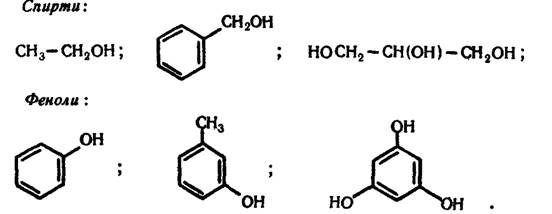
| Текст к ситуации | СПИРТИ, ФЕНОЛИ Спирти і феноли – органічні речовини, молекули яких містять гідроксильні групи –ОН, сполучені з вуглеводневими радикалами. Загальна назва спиртів і фенолів – гідроксильні сполуки. Відмінність спиртів і фенолів полягає в тому, що у фенолах гідроксильні групи сполучені безпосередньо з бензольним ядром. Приклади спиртів і фенолів:
Залежно від числа гідроксильних груп, що містяться в молекулі, розрізняють одноатомні, двохатомні, трьохатомні спирти і феноли:
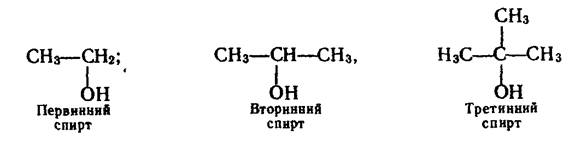
Спирти поділяють також на первинні, в яких гідроксильна група сполучена з первинним карбоновим атомом, вторинні – група –ОН приєднана до вторинного атома Карбону і третинні – група –ОН знаходиться біля третинного Карбону. Приклади таких спиртів:
До простих ефірів належать сполуки, в яких атом Оксигену сполучений з двома вуглецевими радикалами, наприклад СН3–О–С2Н5. НОМЕНКЛАТУРА ТА ІЗОМЕРІЯ ГІДРОКСИЛЬНИХ СПОЛУКНоменклатура. За міжнародною номенклатурою назви спиртів утворюють від назв відповідних алканів з додаванням закінчення -ол. Після закінчення зазначають номер атома Карбону, біля якого знаходиться гідроксильна група. Нумерацію атомів Карбону починають з того кінця ланцюга, до якого ближче розташована гідроксильна група. У назви двохатомних та інших багатоатомних спиртів перед закінченням -ол додають префікс ди- (ді-), три- і т. Д. Залежно від кількості груп. Перед назвою основного ланцюга зазначають положення всіх груп. Для деяких спиртів поширені назви за раціональною номенклатурою. Ці назви утворюють з назви радикала і слова "спирт", наприклад: СН3ОН – метиловий спирт, С2Н5ОН – етиловий спирт, (СН3)2СНОН – ізопропіловий спирт Приклади:
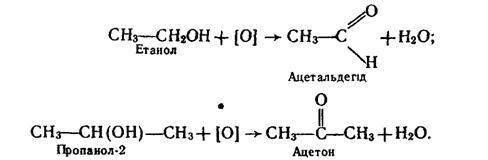
Ізомерія. Ізомерія спиртів пов`язана як з розгалуженням вуглецевого ланцюга, так і з різним положенням гідроксильної групи. Наприклад, бутанол С4Н9ОН може мати такі ізомери; Наведені ізомери різняться властивостями, наприклад температурами кипіння, які дорівнюють 117,3°С (бутанол-1); 99,5°С (бутанол-2); 108,4°С (2-метилпропанол-1); 82,5°С (2-метилпропанол-2). НАСИЧЕНІ ОДНОАТОМНІ СПИРТИ До насичених одноатомних спиртів належать аліфатичні спирти, молекули яких містять одну гідроксильну групу, сполучену з алкільним радикалом: R-OH. Гомологічний ряд. Члени гомологічного ряду насичених одноатомних спиртів мають загальну формулу СnН2n+1ОН, де n = 1, 2, 3, 4 …. Першими членами цього ряду є СН3ОН – метанол, С2Н5ОН – етанол, С3Н7ОН – пропанол, С4Н9ОН – бутанол. Властивості. За звичайних умов насичені одноатомні спирти з нормальною будовою ланцюга, що містять від 1 до 11 атомів Карбону, – це безбарвні рідини. Зі збільшенням молекулярної маси спиртів їх розчинність у воді зменшується: метанол, етанол і пропанол змішуються з водою в будь-яких співвідношеннях, бутанол та інші рідкі за звичайних умов спирти розчиняються у воді мало, а вищі спирти практично не розчиняються у воді. Спирти мають досить високі температури кипіння. Це пов`язано з асоціацією їх молекул, яка відбувається так само, як і асоціація молекул води, за рахунок утворення водневих зв`язків між молекулами RОН (R – вуглеводневий радикал). Хімічні властивості спиртів обумовлені переважно наявністю гідроксильної групи в молекулі. 1. Взаємодія з лужними металами. Під дією лужних металів на спирти утворюються алкоголяти: 2С2Н5–ОН +2Nа ® 2С2Н5–ОNа + Н2. Ця реакція відбувається з розривом зв`язку О–Н у гідроксильній групі. 2. Взаємодія з галогеноводнями (гідрогенгалогенідами) та іншими галогеновмісними речовинами. Під дією галогеноводнів або хлоридів Фосфору РСl5, РСl3 на насичені одноатомні спирти відбувається заміщення групи ОН у спиртах на галоген, наприклад: С2Н5ОН + НВr ® С2Н5Вr + Н2О. Ця реакція за участю гідроксильної групи відбувається з розривом зв`язку С–О. 3. Дегідратація. При наявності фосфатної або концентрованої сульфатної кислоти при нагріванні від спиртів відщеплюється вода і утворюються ненасичені вуглеводні, наприклад: СН3–СН(ОН)–СН3 ––® СН3–СН=СН2 + Н2О Дегідратація спиртів відбувається за правилом Зайцева: атом Гідрогену відщеплюється від сусіднього (до атому Карбону з функціональною групою) менш гідрогенізованого атома Карбону. 4. Взаємодія з кисневмісними кислотами. Спирти реагують з кислотами, утворюючи складні ефіри (естери), які розглянуто далі. Наприклад, під час взаємодії метанолу з нітратною кислотою утворюється складний ефір нітратної кислоти – метилнітрат: СН3ОН + НNО3® СН3–О–NО2 + Н2О Складні ефіри (естери) утворюються також при взаємодії спиртів з органічними кислотами. 5. Окислення. Під час спалювання спиртів (окислення киснем повітря) утворюються Карбон (IV) оксид і вода: 2СН3ОН + 3О2® 2СО2 + 4Н2О. При каталітичному окисленні киснем повітря, окисленні калій перманганатом, калій дихроматом при наявності сульфатної кислоти утворюються альдегіди і кетони (ці сполуки розглянуто далі), наприклад:
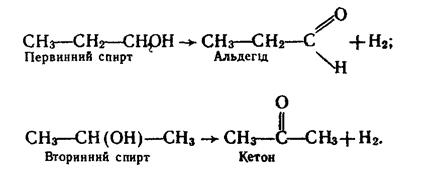
При енергійному окисненні первинних спиртів сильними окисниками утворюються карбонові кислоти. Третинні спирти більш стійкі до окислення. Тільки під дією сильних окислювачів вони можуть окислюватися з розщепленням вуглецевого ланцюга. 6. Дегідрування. Під час каталітичного дегідрування первинних спиртів утворюються альдегіди, вторинних спиртів – кетони: Каталізатором дегідрування спиртів звичайно є мідь (температура 300°С).
Добування. Насичені спирти можна добути гідролізом галогенопохідних відповідних алканів водним розчином лугу, наприклад: С4Н9Вr + Н2О ––® С4Н9ОН + НВr. Спирти утворюються також при гідратації алкенів (за правилом Марковнікова): СН3–СН=СН2 + Н2О ® СН3–СН(ОН)–СН3. Спирти можна добути відновленням інших оксигеновмісних сполук – альдегідів і кетонів. Інші методи добування спиртів розглянуто при вивченні окремих представників гомологічного ряду. Метанол. Метанол, або метиловий спирт, СН3ОН – безбарвна рідина з характерним запахом спиртів. Дуже отруйний. Найважливіший промисловий метод добування метанолу грунтується на використанні синтез-газу (суміш СО з Н2), який добувають конверсією метану з водяною парою. Для добування метанолу синтез-газ пропускають над каталізатором (сумішшю оксидів Купруму, Цинку і Алюмінію) при температурі СО + 2Н2® СН3ОН. Старий метод промислового добування метанолу полягає в сухій перегонці деревини, внаслідок чого спирт дістав назву деревного. Метанол – важливий продукт хімічної промисловості. У великих кількостях його переробляють на формальдегід. З нього добувають і інші органічні речовини, наприклад ефіри кислот. Метанол використовують у промисловому органічному синтезі як метилюючий агент (для введення метильної групи в різні сполуки). Метанол застосовують як розчинник у лакофарбовій промисловості, як компонент пального для автомобілів (добавка метанолу до бензину підвищує октанове число пального). Етанол. Етанол, або етиловий спирт, С2Н5ОН – безбарвна рідина з характерним запахом. Тривіальна назва етанолу – винний спирт. Основним промисловим методом добування етанолу є каталітична гідратація етилену. Реакція відбувається над каталізатором на основі фосфатної кислоти при температурі 260–300°С і тиску 7–8 МПа: С2Н4 + Н2О –––® С2Н5ОН Етанол утворюється під час бродіння продуктів, що містять крохмаль і цукристі речовини (зерна, фруктів, овочів). Бродіння – складний процес. Сумарну реакцію, яка відбувається під час бродіння поширеної цукристої речовини – глюкози С6Н12О6, можна виразити рівнянням: С6Н12О6® 2С2Н5ОН + 2СО2 Недоліком цього методу добування спирту е використання харчової сировини. Як сировину для добування етанолу можна використати деревину, що містить целюлозу. Під час гідролізу целюлози утворюється глюкоза, зброджуванням якої добувають етанол. Етанол є одним з великотоннажних продуктів промислового органічного синтезу. Він застосовується у виробництві оцтової кислоти, 1,3-бутадієну, ефірів. Як розчинник етанол застосовують у лакофарбовій промисловості. У великих кількостях його використовують у виробництві ліків і в харчовій промисловості. З технічною метою часто застосовують денатурований спирт – етанол з домішкою речовин, шкідливих для організму. НАСИЧЕНІ БАГАТОАТОМНІ СПИРТИ Багатоатомні спирти містять у молекулі кілька гідроксильних груп. Двохатомні спирти називають діолами, або гліколями. Назви двохатомних спиртів за міжнародною номенклатурою складають з назви відповідного алкану з додаванням закінчення -діол і цифр, які означають положення гідроксильної групи в ланцюгу. Трьохатомні спирти називають тріолами, або гліцеринами (гліцерилами). Їх назви будують аналогічно до назв двохатомних спиртів, але з додаванням закінчення Найпростіші представники двох- і трьохатомних спиртів:
Властивості. Хімічні властивості багатоатомних спиртів багато в чому подібні до властивостей одноатомних спиртів. При цьому в реакціях може брати участь як одна, так і дві і більше гідроксильних груп. Нижче розглядаються властивості багатоатомних спиртів на прикладі етиленгліколю і гліцерину. Це безбарвні в`язкі сиропоподібні рідини, солодкуваті на смак, добре розчиняються у воді. 1. Взаємодія з лужними металами. Лужні метали витісняють водень з гідроксильних груп з утворенням гліколятів або гліцератів: 2СН2ОН–СН2ОН + Nа ® 2СН2ОН–СН2ОNа + Н2 Моногліколят натрію СН2ОН–СН2ОН + 2Nа ® 2СН2ОNа–СН2ОNа + Н2. Дигліколят натрію Аналогічно реагує з лужними металами гліцерин, при цьому можуть утворюватись моно-, ди- і тригліцерати. 2. Взаємодія з галогеноводнями. Багатоатомні спирти реагують з галогеноводнями (НСl, НВr, НІ) з утворенням галогенозаміщених спиртів або галогенопохідних алканів: СН2ОН–СН2ОН + НВr ® СН2ОН–СН2Вr + Н2О 2 Брометанол або СН2ОН–СН2ОН + 2НВr ® СН2Вr–СН2Вr + Н2О 1,2-Диброметан 3. Взаємодія з кислотами. З кислотами багатоатомні спирти утворюють складні ефіри (естери), наприклад: СН2ОН–СНОН–СН2ОН + 3НNО3® СН2ОNО2–СНОNО2–СН2ОNО2 + 3Н2О Гліцерин Нітрогліцерин Складні ефіри гліцерину з органічними кислотами називають жирами.
У записаних формулах гліколяту і гліцерату міді (II) стрілками показані донорно-акцепторні зв`язки (Сu – акцептор). Сполуки такого типу належать до комплексних. Добування і застосування етиленгліколю і гліцерину. Етиленгліколь добувають у промисловості гідратацією (приєднання води) етиленоксиду: Н2С–СН2 + Н2О ® СН2ОН–СН2ОН. \ / О Етиленоксид Як і одноатомні спирти, етиленгліколь можна добути гідролізом галогенопохідних алканів водним розчином лугів. Для цієї реакції необхідні СН2Сl–СН2Сl + 2Н2О ® СН2ОН–СН2ОН + 2НСl. 1,2-Дихлоретан Етиленгліколь утворюється під час пропускання етилену крізь розчин перманганату калію, при цьому відбуваються окислення і гідратація етилену:
СН2=СН2 + [О] + Н2О ® СН2ОН–СН2ОН. Гліцерин добувають синтетично з пропілену за такою схемою: Гліцерин входить до складу природних сполук – жирів рослинного і тваринного походження– і може бути виділений з них. Етиленгліколь і гліцерин використовуються в промисловому органічному синтезі. Гліцерин застосовують для виробництва мастил, як зм`якшувач шкіри і тканин, у парфюмерній, фармацевтичній і харчовій промисловості. Водні розчини етиленгліколю і гліцерину замерзають при низьких температурах, тому їх використовують як антифризи – рідини з низькою температурою замерзання, які застосовуються для охолодження двигунів внутрішнього згоряння. |
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 102 |
| Текст к ситуации | КАРБОНІЛЬНІ СПОЛУКИ Карбонільні сполуки містять у молекулі карбонільну групу С=О. Карбонільні сполуки поділяють на альдегіди і кетони. АЛЬДЕГІДИ. НОМЕНКЛАТУРА, ВЛАСТИВОСТІ І ДОБУВАННЯУ молекулах альдегідів карбонільна група сполучена з вуглеводневим радикалом і атомом Гідрогену (або з двома атомами Гідрогену), тобто загальна формула цих сполук
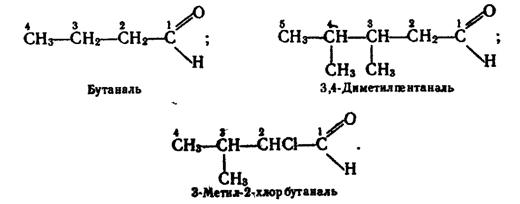
Номенклатура. Назви альдегідів за замісниковою номенклатурою згідно з правилами ІUРАК будують з назви відповідного вуглеводню з додаванням закінчення -аль. Перед коренем назви записують бічні замісники, зазначаючи їх положення і кількість. Нумерацію атомів Карбону починають з атома карбонільної групи. Приклади:
Для альдегідів широко використовують тривіальні назви, які аналогічні назвам відповідних органічних кислот (вони розглядаються далі). У табл.3 наведено назви за замісниковою номенклатурою та тривіальні назви деяких насичених альдегідів. Як видно з табл.3, починаючи з четвертого члена ряду насичених альдегідів, існують ізомери, які різняться розгалуженістю вуглецевого ланцюга. Таблиця 3. Деякі насичені альдегіди
Властивості. Перший член гомологічного ряду насичених альдегідів НСНО – безбарвний газ, кілька наступних альдегідів – рідини. Вищі альдегіди – тверді речовини. У карбонільній групі зв`язок між атомами Оксигену і Карбону сильно полярний: електронна густина зміщена в бік атома кисню
Для карбонільних сполук характерні реакції нуклеофільного приєднання. В цих реакціях нуклеофільні агенти (негативно заряджені частинки) приєднуються до атома Карбону карбонільної групи, а електрофільні агенти (позитивно заряджені частинки) приєднуються до атома Оксигену. Вплив атома Оксигену в карбонільних сполуках передається по ланцюгу. Наприклад, у сполуці, що має фрагмент
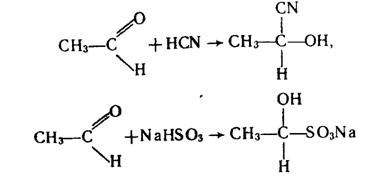
внаслідок зміщення електронної густини до Оксигену атом Гідрогену, сполучений з другим атомом Карбону, виявлятиме підвищену рухливість – його легко відірвати або замістити. Отже, карбонільна група обумовлює високу реакційну здатність альдегідів. 1. Реакції приєднання. Альдегіди легко приєднують ціановодень НСN і гідросульфіт натрію NаНSО3:
Продукти приєднання NаНSО3 – кристалічні речовини, розчинні у воді. При нагріванні з кислотами вони розпадаються з утворенням вихідного альдегіду. Тому останню реакцію використовують для очистки альдегідів. При наявності нікелевих або платинових каталізаторів альдегіди приєднують водень і відновлюються до первинних спиртів, наприклад:
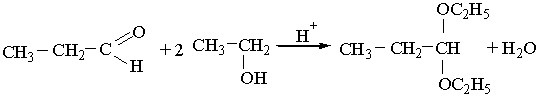
Приєднуючи спирти, альдегіди утворюють сполуки, що мають назву ацеталів. Реакція відбувається при наявності кислот:
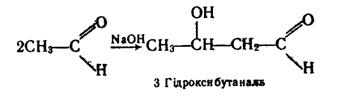
Ацеталі — це прості ефіри двохатомного спирту. Вони легко гідролізуються з утворенням вихідних речовин. 2. Реакції полімеризації і конденсації. Ці реакції характерні для альдегідів і обумовлені реакційною здатністю карбонільної групи. Процеси полімеризації розглядаються далі, при вивченні властивостей формальдегіду і ацетальдегіду.
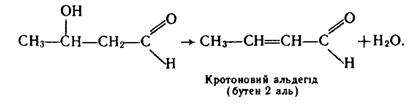
Таку речовину називають альдолем. При відщепленні молекули води від гідроксибутаналю утворюється альдегід, що містить подвійний зв`язок у ланцюгу: .
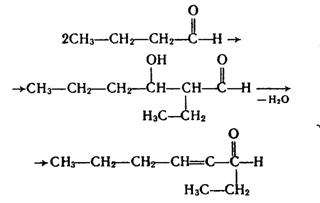
Подібні реакції конденсації альдегідів називаються реакціями альдольно-кротонової конденсації. При конденсації інших альдегідів реакція також завжди відбувається з участю другого атома Карбону однієї з молекул, наприклад:
3. Окислення. Під час окислення альдегідів, яке відбувається дуже легко, утворюються органічні кислоти або їхні солі. Наприклад, під час окислення оцтового альдегіду утворюється оцтова кислота:
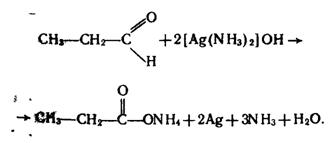
Якісною реакцією на альдегіди є реакція срібного дзеркала – окислення їх аміачним розчином оксиду срібла при нагріванні:
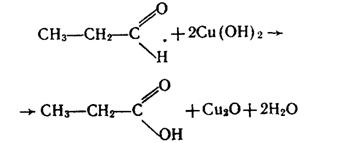
Металічне срібло, яке виділяється, вкриває стінки посудини тонким блискучим шаром. Альдегіди окислюються також Купрум (II) гідроксидом, який відновлюється до червоно-коричневого Купрум (I) оксиду:
4. Заміщення Оксигену карбонільної групи. Атом Оксигену в молекулі альдегіду може бути заміщений на галоген під дією галогенідів Фосфору РСl5 або РВr5, наприклад:
Під дією гідроксиламіну NН2ОН на альдегіди карбонільний Оксиген заміщується на оксімідну групу =N–ОН:
Нітрогеновмісна органічна сполука, що утворюється, належить до оксимів. 5. Взаємодія з галогенами. Як уже зазначалось, атом Гідрогену біля другого атома Карбону вуглеводневого ланцюга альдегідів має підвищену рухливість. Під час взаємодії альдегідів з хлором чи бромом цей водневий атом легко заміщується на галоген, наприклад:
Добування. 1. Альдегіди утворюються під час окислення або каталітичного дегідрування (відщеплення водню) первинних спиртів:
Каталітичне дегідрування спиртів відбувається при наявності металічної міді:
2. Альдегіди можна добути гідролізом дигалогенопохідних алканів, наприклад:
3. Альдегіди утворюються під час взаємодії алкенів з оксидом Карбону(II) і воднем (оксосинтез):
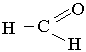
Оксосинтез відбувається при наявності каталізаторів – комплексних сполук кобальту під тиском 5–10 МПа. ФОРМАЛЬДЕГІД, АЦЕТАЛЬДЕГІД, БЕНЗАЛЬДЕГІДФормальдегід. Першим членом гомологічного ряду насичених альдегідів є формальдегід НСНО, який має будову:
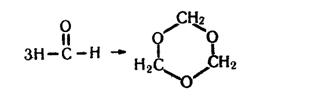
Його називають також метаналем (міжнародні номенклатура) та мурашиним альдегідом. Формальдегід – це безбарвний газ з характерним різким запахом. Добре розчиняється у воді, утворюючи гідрат НСНО·Н2О. Водний розчин з масовою часткою формальдегіду 30–40 % називається формаліном. Формалін є добрим дезинфікуючим та консервуючим засобом. Формальдегід є важливим продуктом хімічної промисловості. Його добувають переважно окисленням метанолу киснем повітря при наявності каталізаторів: 2СН3ОН + О2® 2НСНО + 2Н2О. Формальдегід виявляє загальні властивості альдегідів. Крім того, має і свої особливості. Так, він може самовільно тримеризуватися (сполучення трьох молекул), утворюючи параформальдегід (триоксиметилен):
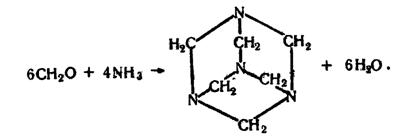
Формальдегід взаємодіє з аміаком, утворюючи циклічну сполуку гексаметилентетрамін, або уротропін:
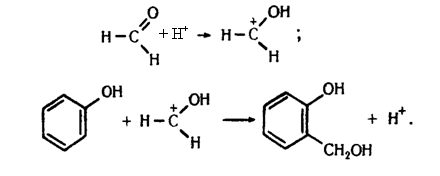
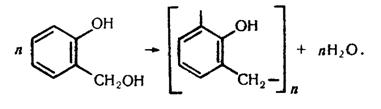
Під дією лугів формальдегід окислюється і відновлюється одночасно, утворюючи метиловий спирт та сіль мурашиної кислоти: 2НСНО + КОН ® СН3ОН + НСООК Формальдегід є сировиною для синтезу ізопрену, з якого добувають штучний каучук. Важлива галузь застосування формальдегіду – виробництво полімерів. Формальдегід полімеризується з утворенням поліформальдегіду, або поліоксиметилену: пНСНО ® (–СН2–О–)n Поліформальдегід належить до гетероланцюгових полімерів, оскільки головний ланцюг його макромолекули містить атоми двох типів: Карбону та Оксигену. Поліформальдегід – безбарвна кристалічна речовина. Він має механічну міцність, є добрим діелектриком. Його використовують у машинобудуванні для виготовлення різних деталей, для добування міцних синтетичних волокон і плівок. Фенолоформальдегідні полімери. Формальдегід при наявності кислот реагує з фенолом. Реакція відбувається зіа такою схемою:
Молекули фенолоспирту, який утворюється, сполучаються між собою з утворенням макромолекул: Продукт, що утворюється, називається фенолоформальдегідним полімером. Реакції утворення полімерів, які супроводжуються виділенням низькомолекулярного продукту, називаються реакціями поліконденсації. Під час полімеризації формальдегіду з фенолом, взятим у надлишку, як правило, утворюються лінійні полімери, які називаються новолачною смолою. Ця смола добре розчиняється в органічних розчинниках, використовується для приготування лаків.
Під час добування резиту до реакційної суміші добавляють різні наповнювачі (скловолокно, азбест тощо), які надають полімеру необхідних властивостей. Загальна назва пластмас, які добувають з фенолоформальдегідного полімеру, – фенопласти. Фенопласти є термореактивними полімерами, вони не плавляться при нагріванні, їх застосовують як конструкційний матеріал. На основі фенопластів добувають легкі пористі матеріали – пінопласти. Ацетальдегід. Ацетальдегід (етаналь, оцтовий альдегід) – це безбарвна, рідина з різким запахом:
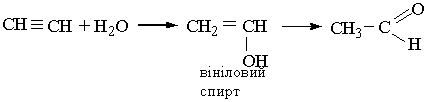
Добре розчиняється у воді. Ацетальдегід у великих кількостях виробляє хімічна промисловість. Основний метод його промислового добування заснований на гідратації ацети-лену. Для цього ацетилен з водяною парою пропускають над каталізатором (НgSО4 з сульфатною кислотою). В результаті приєднання води до ацетилену утворюється вініловий спирт з гідроксильною групою біля подвійного зв`язку. Такі сполуки нестійкі, вініловий спирт піддається перегрупуванню в ацетальдегід:
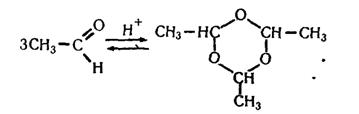
Інший метод добування ацетальдегіду полягає в каталітичному окисленні етилену киснем з участю каталізатора РdСl2 + СuСl2. Ацетальдегід добувають також окисленням чи каталітичним дегідруванням етанолу або ізомеризацією (перетворення на ізомер) етиленоксиду. Для ацетальдегіду характерні всі хімічні властивості альдегідів. Ацетальдегід може тримеризуватися, утворюючи паральдегід:
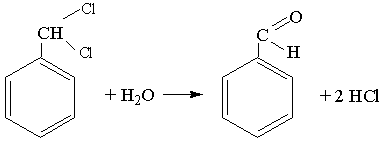
У промисловості основну кількість ацетальдегіду, який виробляють, окислюють до оцтової кислоти. Ацетальдегід використовують і для добування інших органічних продуктів, у тому числі полімерів. Бензальдегід. Бензальдегід С6Н5COH – це безбарвна рідина з запахом гіркого мигдалю, мало розчинна у воді. Бензальдегід добувають лужним гідролізом дихлорпохідної толуену:
Бензальдегід застосовують у виробництві фарб, парфюмерних виробів і в харчовій промисловості. КЕТОНИ У молекулах кетонів карбонільна група сполучена з двома однаковими або різними вуглеводневими радикалами :
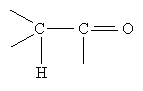
Найпростішим кетоном є ацетон :
Номенклатура. Згідно з міжнародною номенклатурою назви кетонів будують з назв відповідного вуглеводню з додаванням закінчення -он. На початку назви ставлять цифру, що зазначає положення в ланцюгу атома Карбону, з яким сполучений карбонільний кисень. Нумерацію головного ланцюга починають, як завжди, з найбільш розгалуженого кінця вуглецевого ланцюга. Якщо розгалуженість однакова, то нумерують з того кінця ланцюга, до якого ближче розташована карбонільна група. Назви кетонів за раціональною номенклатурою, які також використовуються, будують з назв радикалів, сполучених з карбонільною групою з додаванням слова "кетон". Приклад:
Ізомерія. Ізомерія кетонів обумовлена розгалуженістю вуглецевого ланцюга вуглеводневих радикалів і різним положенням карбонільного Оксигену. Властивості. Простіші кетони є безбарвними рідинами, які розчиняються у воді. Вищі кетони – тверді речовини. Багато які хімічні властивості, характерні для альдегідів, виявляються і у кетонів.
Гідрування кетонів при наявності каталізаторів приводить до утворення вторинних спиртів:
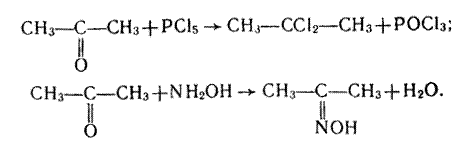
На відміну від альдегідів кетони не взаємодіють із спиртами, не вступають у реакції конденсації і полімеризації. 2. Окислення. Кетони окислюються значно важче, ніж альдегіди, і тільки сильними окислювачами. Під час окислення кетонів відбувається розрив (деструкція) вуглеводневого ланцюга і утворюється суміш продуктів. Кетони не вступають у реакцію срібного дзеркала. 3. Заміщення Оксигену карбонільної групи. Так само, як і в альдегідах, атом Оксигену в молекулі кетону може бути заміщений дією галогенідів фосфору (РСl5, РВr5) або гідроксиламіну NН2ОН: У першій реакції утворюється дигалогенопохідна алкану, в другій – оксим.
4. Взаємодія з галогенами. Як і альдегіди, кетони легко реагують з хлором і бромом. Атом Гідрогену, сполучений з одним із атомів Карбону, сполученим з карбонільною групою, заміщується на галоген:
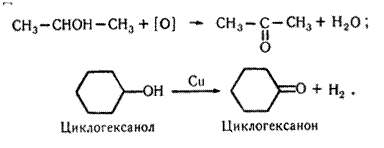
Добування. 1. Кетони утворюються під час окислення або каталітичного дегідрування вторинних спиртів, наприклад: Каталітичне дегідрування проводять з використанням мідних каталізаторів.
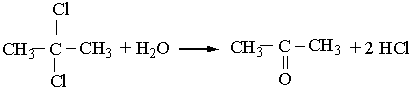
2. Як і альдегіди, кетони можна добути гідролізом дигалогенопохідних алканів. Щоб утворився кетон, обидва атоми галогену у вихідній сполуці повинні знаходитись біля одного (не кінцевого) атома Карбону:
3. Кетони утворюються внаслідок приєднання води до гомологів ацети-лену при наявності каталізаторів – солей Гідраргіруму (II), наприклад: Н3С–СºС—СН3 + Н2О –® СН3–СН2–СО–СН3 Ацетон. Ацетон (пропанон, диметилкетон) – безбарвна рідина з характерним запахом. Температура кипіння ацетону 56,2°С. Добре розчиняється у воді і сам є розчинником органічних сполук. Ацетон – важливий продукт хімічної промисловості. Його добувають разом з фенолом кумольним методом. Інший промисловий спосіб полягає в гідратації пропілену до утворення спирту з наступним його каталітичним дегідруванням або окисленням: СН3–СН=СН2 + Н2О ® СН3–СНОН–СН3; СН3–СНОН–СН3® СН3–СО–СН3+Н2 Ацетон застосовують як розчинник. Він також є вихідною речовиною для синтезу багатьох органічних сполук. Ацетофенон. Ацетофенон (метилфенілкетон) С6Н5–СО–СН3 – безбарвна речовина з температурою плавлення 19,6°С. У воді практично не розчиняється. Має запах черемхи. Застосовується при ви | ||||||||
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 103 |
| Текст к ситуации | КАРБОНОВІ КИСЛОТИ
або спрощено —СООН. Карбоксильна група складається із сполучених карбонільної і гідроксильної груп, що визначило її назву.У карбонових кислотах карбоксильна група сполучена з вуглеводневим радикалом R, тому в загальному вигляді формулу карбонової кислоти можна записати так: R–соон. У карбонових кислотах карбоксильна група може сполучатися з різними вуглеводневими радикалами – насиченими, ненасиченими, ароматичними. У зв`язку з цим виділяють насичені, ненасичені та ароматичні карбонові кислоти, наприклад:
Залежно від числа карбоксильних груп, що містяться в молекулах карбонових кислот, розрізняють одноосновні та двохосновні кислоти, наприклад: Одноосновні кислоти називають також монокарбоновими, а двохосновні – дикарбоновими кислотами.
ГОМОЛОГІЧНИЙ РЯД НАСИЧЕНИХ
| ||||||||||||||||||||||||||||||||
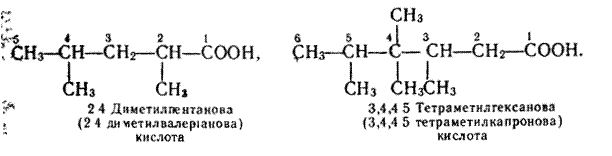 |
Для деяких членів гомологічного ряду насичених карбонових кислот застосовують тривіальні назви. В табл.1 наведено формули деяких насичених одноосновних кислот і їх назви за замісниковою номенклатурою та тривіальні назви.
Таблиця 1. Деякі насичені одноосновні кислоти
| Формула | Назва | |
| за замісниковою номенклатурою | тривіальна | |
| нсоон СН3СООН С2Н5СООН С3Н7СООН С4Н9СООН С5Н11соон С6Н13СООН С15Н31соон С16Н33соон С17Н35соон | Метанова Етанова Пропанова Бутанова Пентанова Гексанова Гептанова Пентадеканова Гексадеканова Гептадеканова | Мурашина Оцтова Пропіонова Масляна Валеріанова Капронова Енантова Пальмітинова Маргаринова Стеаринова |
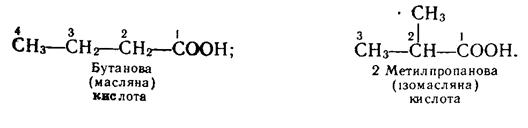 Ізомери. Починаючи з бутанової кислоти С3Н7СООН, члени гомологічного ряду насичених одноосновних кислот мають ізомери, їх ізомерія зумовлена розгалуженістю карбонового ланцюга вуглеводневих радикалів. Так, бутанова кислота має такі два ізомери (у дужках дано тривіальну назву):
Ізомери. Починаючи з бутанової кислоти С3Н7СООН, члени гомологічного ряду насичених одноосновних кислот мають ізомери, їх ізомерія зумовлена розгалуженістю карбонового ланцюга вуглеводневих радикалів. Так, бутанова кислота має такі два ізомери (у дужках дано тривіальну назву):
Формулі С4Н9СООН відповідають чотири ізомерні карбонові кислоти:
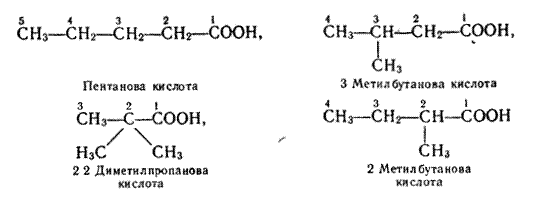
ВЛАСТИВОСТІ І ДОБУВАННЯ НАСИЧЕНИХ ОДНООСНОВНИХ КИСЛОТ
Властивості. Кислоти гомологічного ряду з нормальною будовою від мурашиної до С8Н17СООН (нонанової кислоти) за звичайних умов – безбарвні рідини, що мають різкий запах. Вищі члени ряду, починаючи з С9Н19СООН, – тверді речовини. Мурашина, оцтова і пропіонова кислоти добре розчиняються у воді, змішуються з нею в будь-яких співвідношеннях. Інші рідкі кислоти обмежено розчиняються у воді. Тверді кислоти у воді практично нерозчинні.
Особливості хімічних властивостей карбонових кислот зумовлені сильним взаємним впливом карбонільної (=С=О) і гідроксильної (–О–Н) груп.
У карбоксильній групі зв`язок між Карбоном і карбонільним Оксигеном сильнополярний. Проте, позитивний заряд на атомі Карбону частково зменшується внаслідок притягання електронів атома Оксигену гідроксильної групи. Тому в карбонових кислотах карбонільний Карбон менш схильний до взаємодії з нуклеофільними частинками, ніж в альдегідах і кетонах.
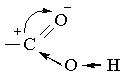 З іншого боку, під впливом карбонільної групи підсилюється полярність зв`язку О–Н за рахунок зміщення електронної густини від Оксигену до атома Карбону. Всі зазначені особливості карбоксильної групи можна проілюструвати такою схемою:
З іншого боку, під впливом карбонільної групи підсилюється полярність зв`язку О–Н за рахунок зміщення електронної густини від Оксигену до атома Карбону. Всі зазначені особливості карбоксильної групи можна проілюструвати такою схемою:
Розглянутий характер електронної будови карбоксильної групи зумовлює відносну легкість відщеплення атома водню цієї групи. Тому у карбонових кислот добре виявлені кислотні властивості. У безводному стані і особливо у водних розчинах карбонові кислоти дисоціюють на іони:
СН3–СН2–СООН ↔ СН3–СН2–СОО– + Н+.
Кислотний характер розчинів карбонових кислот можна встановити за допомогою індикаторів. Карбонові кислоти є слабкими електролітами, причому сила карбонових кислот зменшується зі збільшенням молекулярної маси кислоти.
Для насичених одноосновних кислот найбільш характерні реакції, зумовлені кислотними властивостями, а також реакції заміщення гідроксильної групи.
1. Взаємодія з металами. Карбонові кислоти реагують з деякими металами з утворенням солей і водню. Наприклад, утворення магній ацетату:
2СН3СООН + Мg ® Мg(СН3СОО)2 + Н2
2. Взаємодія з основними оксидами і основами. Як усі кислоти, карбоксильні сполуки реагують з основними оксидами і основами, наприклад:
2С2Н5СООН + МgО ® Мg(С2Н5СОО)2 + Н2О
С2Н5СООН + КОН ® С2Н5СООК + Н2О
3 водним розчином аміаку, який виявляє властивості основ, карбонові кислоти також утворюють солі:
С2Н5СООН + NН3® С2Н5СООNН4
3. Взаємодія зі спиртами. Карбонові кислоти реагують зі спиртами при наявності сильних неорганічних кислот. Від молекули кислоти відщеплюється група ОН, від молекули спирту – атом Н, в результаті утворюються складні ефіри:
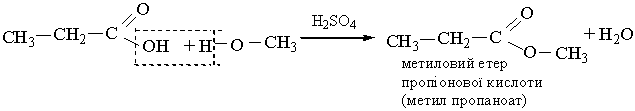 |
4. Взаємодія з галогенідами Фосфору і Сульфуру. Галогеніди РСl5, РСl3 і SОСl2 взаємодіють з карбоновими кислотами, утворюючи хлорангідриди кислот, наприклад:
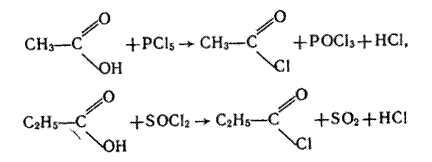 |
5. Взаємодія з водовідбирними агентами. Під дією сильних водовідбирних речовин, наприклад Р2О5, на карбонові кислоти утворюються ангідриди кислот:
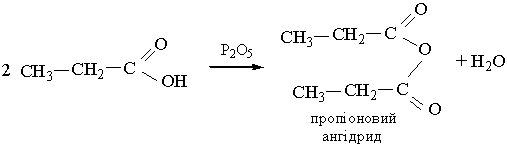 |
6. Взаємодія з галогенами. Як і в альдегідах, Хлор і Бром можуть заміщувати атом Гідрогену біля другого карбонового атома з утворенням галогенозаміщених кислот, наприклад:
СН3–СН2–СООН + Вr2® СН3–СНВr–СООН + НВr
7. Відновлення і каталітичне гідрування. Відновлюючи карбонові кислоти, можна добути альдегіди і первинні спирти, наприклад:
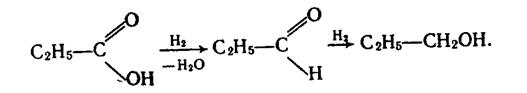 |
Відновлення кислот відбувається дуже важко.
Добування. Основні методи добування карбонових кислот такі.
1. Окислення первинних спиртів і альдегідів. Спирти і альдегіди окислюються досить легко, наприклад:
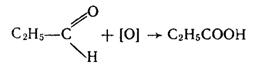 |
Під час окислення кетонів, вторинних і третинних спиртів у жорстких умовах (сильні окислювачі, нагрівання) відбувається розщеплення вуглецевого ланцюга молекул і утворюється, як правило, суміш карбонових кислот. Наприклад, окислюючи ацетон, можна добути суміш мурашиної і оцтової кислот.
2. Окислення алканів. Суміш нижчих алканів (бутан–октан) окислюється при наявності каталізаторів переважно до оцтової кислоти. Алкани, що містять 9–20 атомів Карбону, окислюються до вищих кислот.
3. Гідроліз нітрилів. Нітрили – сполуки типу R–СºN. Під час нагрівання нітрилів з водою, в яку добавлено неорганічні кислоти, утворюються карбонові кислоти, наприклад, при гідролізі акрилонітрилу утворюється акрилова кислота (пропенова):
СН3–СºN + 2Н2О ® СН3–СООН + NН3
4. Карбонілування алкенів. Кислоти, починаючи з пропіонової, можна добути приєднанням оксиду Карбону (II) і води до алкенів. Каталізатором реакції є фосфорна кислота, процес відбувається при температурі 300–350°С і тиску 20–30 МПа. Приклад:
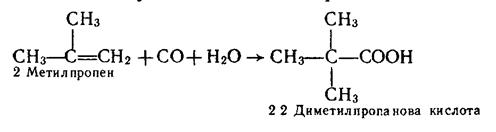 |
МУРАШИНА, ОЦТОВА ТА ВИЩІ НАСИЧЕНІ КИСЛОТИ
Мурашина кислота. Перший член гомологічного ряду насичених одноосновних карбонових кислот – мурашина (метанова) кислота НСООН:
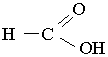
Це безбарвна рідина з різким запахом. Температура кипіння мурашиної кислоти становить 100,7°С.
Мурашина кислота міститься в їдкій речовині, яку виділяють мурашки (цим пояснюється назва кислоти). Вона міститься також у деяких рослинах, наприклад у кропиві. При потраплянні на шкіру викликає опіки.
Мурашина кислота є важливим продуктом хімічної промисловості. Основний метод добування заснований на пропусканні Карбон (II) оксиду крізь концентрований розчин Натрій гідроксиду при температурі ~200°С і тиску
1,2–1,5МПа. При цьому утворюється форміат натрію (сіль кислоти), який обробляють сірчаною кислотою:
NаОН + СО ® НСООNа;
2НСООNа + Н2SО4® 2НСООН + Nа2SО4.
У молекулі мурашиної кислоти карбоксильна група сполучена не з вуглеводневим радикалом а з атомом Гідрогену. Це надає кислоті ряд властивостей, що відрізняють її від інших карбонових кислот. Наприклад, вона найсильніша з одноосновних насичених карбонових кислот. На відміну від інших кислот гомологічного ряду мурашина кислота може бути відновником. Як і альдегіди, вона вступає в реакцію срібного дзеркала з аміачним розчином Аргентум оксиду:
НСООН + 2[Аg(NН3)2]ОН ® СО2 + 2Аg + 4NН3 + 2Н2О.
Мурашина кислота окиснюється сульфатною кислотою (концентрованою) до Карбон (II) оксиду.
Мурашину кислоту застосовують у ряді органічних синтезів, у медицині, в текстильній промисловості, як відновник.
Оцтова кислота. Оцтова (етанова) кислота СН3СООН – безбарвна рідина з характерним різким запахом. Температура кипіння 118,1°С. При температурі 16,75°С кислота твердне, утворюючи кристали, схожі на лід. Тому безводну оцтову кислоту називають льодяною оцтовою кислотою.
Добре розчиняється у воді. Її 70–80 %-й розчин називається оцтовою есенцією, а 3–6 %-й – оцтом.
Ця кислота трапляється в природі. Вона міститься у багатьох тваринних і рослинних організмах, утворюється під час скисання багатьох продуктів і вина.
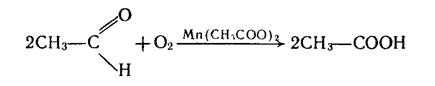 Оцтова кислота є важливим продуктом хімічної промисловості. Її добувають окисленням ацетальдегіду киснем повітря. Процес здійснюють при наявності каталізатора [манган (II) ацетату Мn(СН3СОО)2] і температурі 50–60°С:
Оцтова кислота є важливим продуктом хімічної промисловості. Її добувають окисленням ацетальдегіду киснем повітря. Процес здійснюють при наявності каталізатора [манган (II) ацетату Мn(СН3СОО)2] і температурі 50–60°С:
Оцтову кислоту синтезують також з метанолу та Карбон (II) оксиду за реакцією:
СН3ОН + СО ® СН3СООН.
Оцтова кислота є проміжним продуктом синтезу багатьох органічних речовин, барвників, штучних волокон. Її використовують також у харчових цілях для консервування продуктів і як приправу.
Вищі насичені кислоти. З вищих одноосновних насичених кислот найбільше значення мають пальмітинова кислота С15Н31СООН і стеаринова кислота С17Н35СООН. Це безбарвні тверді речовини, не розчинні у воді.
Стеаринову і пальмітинову кислоти можна виділити з рослинних і тваринних жирів. У промисловості ці кислоти добувають окисленням парафіну, який виділяють з нафти.
Стеаринова і пальмітинова кислоти виявляють багато властивостей, характерних для карбонових кислот. Практичне значення має реакція їх з лугами з утворенням солей. Солі стеаринової та пальмітинової кислот – основні компоненти мила. Стеаринову та пальмітинову кислоти застосовують у виробництві мийних засобів, лаків, фарб, лінолеуму, гуми.
До вищих ненасичених кислот належить олеїнова кислота С17Н33СООН, яка містить один подвійний зв’язок між 9 та 10 атомами Карбону. Тому олеїнова кислота реагує з бромною водою, приєднуючи бром по місцю подвійного зв’язку. При каталічному приєднанні водню утворюється стеаринова кислота.
| 1 | Продовжити виконання лабораторної роботи | 2 |
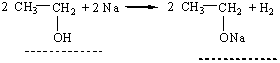
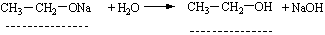
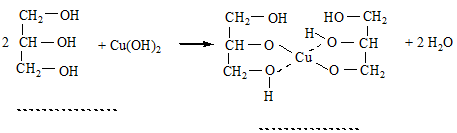
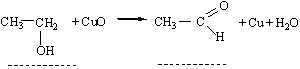
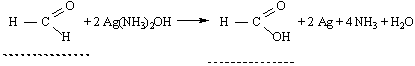
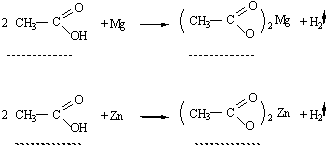
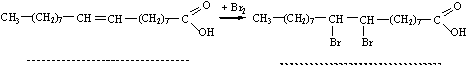
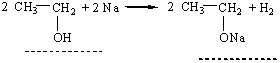
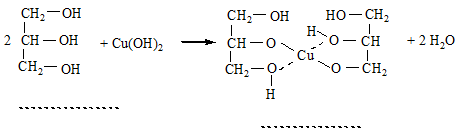
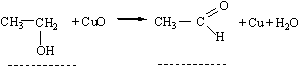
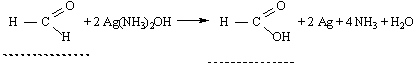
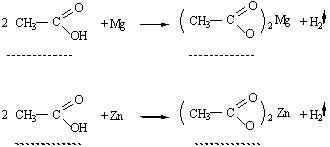
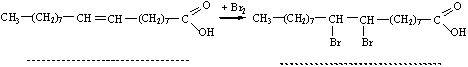
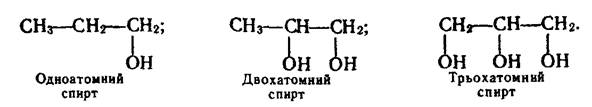
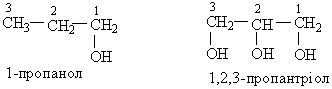

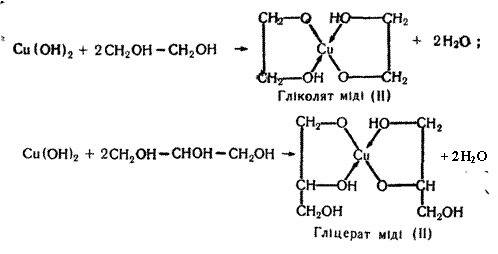 4. Взаємодія з Купрум (II) гідроксидом. Ця реакція характерна тільки для багатоатомних спиртів. Осад Купрум (II) гідроксиду розчиняється в етиленгліколі та гліцерині з утворенням розчину яскраво-синього кольору:
4. Взаємодія з Купрум (II) гідроксидом. Ця реакція характерна тільки для багатоатомних спиртів. Осад Купрум (II) гідроксиду розчиняється в етиленгліколі та гліцерині з утворенням розчину яскраво-синього кольору:
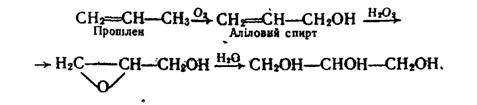
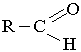
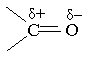
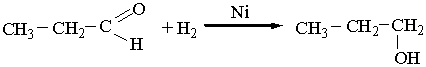
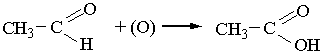
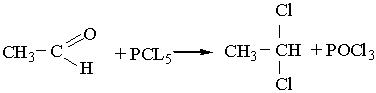
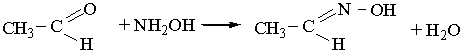
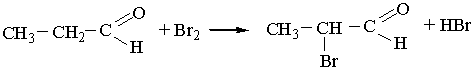
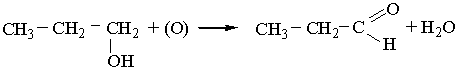
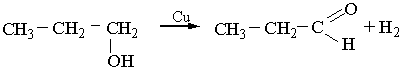
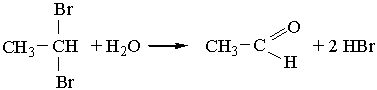
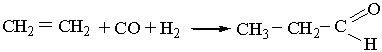
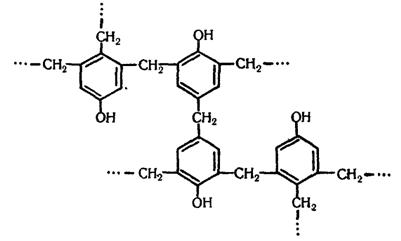
 Якщо поліконденсація йде при надлишку формальдегіду, то утворюється резит – полімер, що має складну просторову структуру:
Якщо поліконденсація йде при надлишку формальдегіду, то утворюється резит – полімер, що має складну просторову структуру:
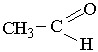
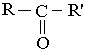
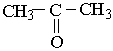
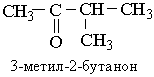
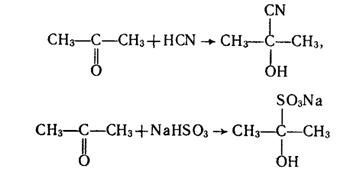 1. Реакції приєднання. Так само, як і альдегіди, кетони приєднують речовини, що містять нуклеофільні частинки, наприклад ціановодень і гідросульфіт натрію:
1. Реакції приєднання. Так само, як і альдегіди, кетони приєднують речовини, що містять нуклеофільні частинки, наприклад ціановодень і гідросульфіт натрію:
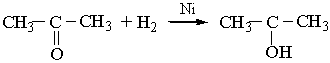
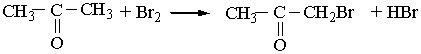
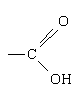 Карбоновими кислотами називаються органічні речовини, до складу яких входить карбоксильна група
Карбоновими кислотами називаються органічні речовини, до складу яких входить карбоксильна група