СПИРТИ, ФЕНОЛИ
Спирти і феноли – органічні речовини, молекули яких містять гідроксильні групи –ОН, сполучені з вуглеводневими радикалами. Загальна назва спиртів і фенолів – гідроксильні сполуки.
Відмінність спиртів і фенолів полягає в тому, що у фенолах гідроксильні групи сполучені безпосередньо з бензольним ядром. Приклади спиртів і фенолів:
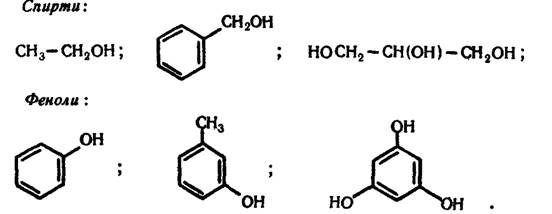
Залежно від числа гідроксильних груп, що містяться в молекулі, розрізняють одноатомні, двохатомні, трьохатомні спирти і феноли:
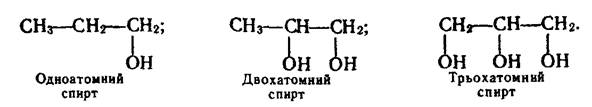
Спирти поділяють також на первинні, в яких гідроксильна група сполучена з первинним карбоновим атомом, вторинні – група –ОН приєднана до вторинного атома Карбону і третинні – група –ОН знаходиться біля третинного Карбону. Приклади таких спиртів:
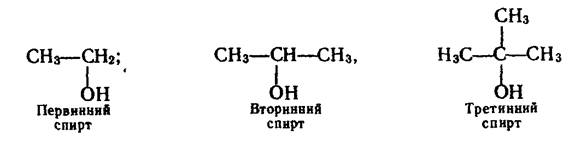
До простих ефірів належать сполуки, в яких атом Оксигену сполучений з двома вуглецевими радикалами, наприклад СН3–О–С2Н5.
НОМЕНКЛАТУРА ТА ІЗОМЕРІЯ ГІДРОКСИЛЬНИХ СПОЛУК
Номенклатура. За міжнародною номенклатурою назви спиртів утворюють від назв відповідних алканів з додаванням закінчення -ол. Після закінчення зазначають номер атома Карбону, біля якого знаходиться гідроксильна група. Нумерацію атомів Карбону починають з того кінця ланцюга, до якого ближче розташована гідроксильна група. У назви двохатомних та інших багатоатомних спиртів перед закінченням -ол додають префікс ди- (ді-), три- і т. Д. Залежно від кількості груп. Перед назвою основного ланцюга зазначають положення всіх груп.
Для деяких спиртів поширені назви за раціональною номенклатурою. Ці назви утворюють з назви радикала і слова "спирт", наприклад: СН3ОН – метиловий спирт, С2Н5ОН – етиловий спирт, (СН3)2СНОН – ізопропіловий спирт
Приклади:
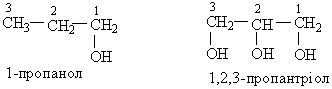
Ізомерія. Ізомерія спиртів пов`язана як з розгалуженням вуглецевого ланцюга, так і з різним положенням гідроксильної групи. Наприклад, бутанол С4Н9ОН може мати такі ізомери;
Наведені ізомери різняться властивостями, наприклад температурами кипіння, які дорівнюють 117,3°С (бутанол-1); 99,5°С (бутанол-2); 108,4°С (2-метилпропанол-1); 82,5°С (2-метилпропанол-2).
НАСИЧЕНІ ОДНОАТОМНІ СПИРТИ
До насичених одноатомних спиртів належать аліфатичні спирти, молекули яких містять одну гідроксильну групу, сполучену з алкільним радикалом: R-OH.
Гомологічний ряд. Члени гомологічного ряду насичених одноатомних спиртів мають загальну формулу СnН2n+1ОН, де n = 1, 2, 3, 4 …. Першими членами цього ряду є СН3ОН – метанол, С2Н5ОН – етанол, С3Н7ОН – пропанол, С4Н9ОН – бутанол.
Властивості. За звичайних умов насичені одноатомні спирти з нормальною будовою ланцюга, що містять від 1 до 11 атомів Карбону, – це безбарвні рідини. Зі збільшенням молекулярної маси спиртів їх розчинність у воді зменшується: метанол, етанол і пропанол змішуються з водою в будь-яких співвідношеннях, бутанол та інші рідкі за звичайних умов спирти розчиняються у воді мало, а вищі спирти практично не розчиняються у воді.
Спирти мають досить високі температури кипіння. Це пов`язано з асоціацією їх молекул, яка відбувається так само, як і асоціація молекул води, за рахунок утворення водневих зв`язків між молекулами RОН (R – вуглеводневий радикал).
Хімічні властивості спиртів обумовлені переважно наявністю гідроксильної групи в молекулі.
1. Взаємодія з лужними металами. Під дією лужних металів на спирти утворюються алкоголяти:
2С2Н5–ОН +2Nа ® 2С2Н5–ОNа + Н2.
Ця реакція відбувається з розривом зв`язку О–Н у гідроксильній групі.
2. Взаємодія з галогеноводнями (гідрогенгалогенідами) та іншими галогеновмісними речовинами. Під дією галогеноводнів або хлоридів Фосфору РСl5, РСl3 на насичені одноатомні спирти відбувається заміщення групи ОН у спиртах на галоген, наприклад:
С2Н5ОН + НВr ® С2Н5Вr + Н2О.
Ця реакція за участю гідроксильної групи відбувається з розривом зв`язку С–О.
3. Дегідратація. При наявності фосфатної або концентрованої сульфатної кислоти при нагріванні від спиртів відщеплюється вода і утворюються ненасичені вуглеводні, наприклад:
СН3–СН(ОН)–СН3 ––® СН3–СН=СН2 + Н2О
Дегідратація спиртів відбувається за правилом Зайцева: атом Гідрогену відщеплюється від сусіднього (до атому Карбону з функціональною групою) менш гідрогенізованого атома Карбону.
4. Взаємодія з кисневмісними кислотами. Спирти реагують з кислотами, утворюючи складні ефіри (естери), які розглянуто далі. Наприклад, під час взаємодії метанолу з нітратною кислотою утворюється складний ефір нітратної кислоти – метилнітрат:
СН3ОН + НNО3® СН3–О–NО2 + Н2О
Складні ефіри (естери) утворюються також при взаємодії спиртів з органічними кислотами.
5. Окислення. Під час спалювання спиртів (окислення киснем повітря) утворюються Карбон (IV) оксид і вода:
2СН3ОН + 3О2® 2СО2 + 4Н2О.
При каталітичному окисленні киснем повітря, окисленні калій перманганатом, калій дихроматом при наявності сульфатної кислоти утворюються альдегіди і кетони (ці сполуки розглянуто далі), наприклад:
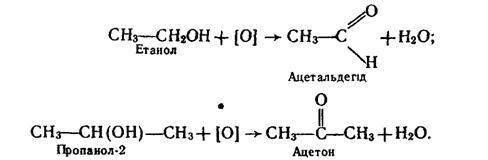
При енергійному окисненні первинних спиртів сильними окисниками утворюються карбонові кислоти.
Третинні спирти більш стійкі до окислення. Тільки під дією сильних окислювачів вони можуть окислюватися з розщепленням вуглецевого ланцюга.
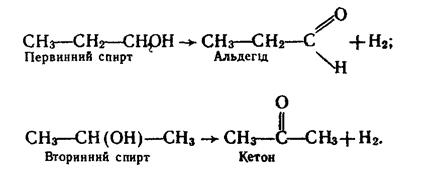
6. Дегідрування. Під час каталітичного дегідрування первинних спиртів утворюються альдегіди, вторинних спиртів – кетони:
Каталізатором дегідрування спиртів звичайно є мідь (температура 300°С).
Добування. Насичені спирти можна добути гідролізом галогенопохідних відповідних алканів водним розчином лугу, наприклад:
С4Н9Вr + Н2О ––® С4Н9ОН + НВr.
Спирти утворюються також при гідратації алкенів (за правилом Марковнікова):
СН3–СН=СН2 + Н2О ® СН3–СН(ОН)–СН3.
Спирти можна добути відновленням інших оксигеновмісних сполук – альдегідів і кетонів.
Інші методи добування спиртів розглянуто при вивченні окремих представників гомологічного ряду.
Метанол. Метанол, або метиловий спирт, СН3ОН – безбарвна рідина з характерним запахом спиртів. Дуже отруйний.
Найважливіший промисловий метод добування метанолу грунтується на використанні синтез-газу (суміш СО з Н2), який добувають конверсією метану з водяною парою. Для добування метанолу синтез-газ пропускають над каталізатором (сумішшю оксидів Купруму, Цинку і Алюмінію) при температурі
200–300°С і тиску 6–8 МПа:
СО + 2Н2® СН3ОН.
Старий метод промислового добування метанолу полягає в сухій перегонці деревини, внаслідок чого спирт дістав назву деревного.
Метанол – важливий продукт хімічної промисловості. У великих кількостях його переробляють на формальдегід. З нього добувають і інші органічні речовини, наприклад ефіри кислот. Метанол використовують у промисловому органічному синтезі як метилюючий агент (для введення метильної групи в різні сполуки).
Метанол застосовують як розчинник у лакофарбовій промисловості, як компонент пального для автомобілів (добавка метанолу до бензину підвищує октанове число пального).
Етанол. Етанол, або етиловий спирт, С2Н5ОН – безбарвна рідина з характерним запахом. Тривіальна назва етанолу – винний спирт.
Основним промисловим методом добування етанолу є каталітична гідратація етилену. Реакція відбувається над каталізатором на основі фосфатної кислоти при температурі 260–300°С і тиску 7–8 МПа:
С2Н4 + Н2О –––® С2Н5ОН
Етанол утворюється під час бродіння продуктів, що містять крохмаль і цукристі речовини (зерна, фруктів, овочів). Бродіння – складний процес. Сумарну реакцію, яка відбувається під час бродіння поширеної цукристої речовини – глюкози С6Н12О6, можна виразити рівнянням:
С6Н12О6® 2С2Н5ОН + 2СО2
Недоліком цього методу добування спирту е використання харчової сировини.
Як сировину для добування етанолу можна використати деревину, що містить целюлозу. Під час гідролізу целюлози утворюється глюкоза, зброджуванням якої добувають етанол.
Етанол є одним з великотоннажних продуктів промислового органічного синтезу. Він застосовується у виробництві оцтової кислоти, 1,3-бутадієну, ефірів. Як розчинник етанол застосовують у лакофарбовій промисловості. У великих кількостях його використовують у виробництві ліків і в харчовій промисловості. З технічною метою часто застосовують денатурований спирт – етанол з домішкою речовин, шкідливих для організму.
НАСИЧЕНІ БАГАТОАТОМНІ СПИРТИ
Багатоатомні спирти містять у молекулі кілька гідроксильних груп.
Двохатомні спирти називають діолами, або гліколями. Назви двохатомних спиртів за міжнародною номенклатурою складають з назви відповідного алкану з додаванням закінчення -діол і цифр, які означають положення гідроксильної групи в ланцюгу.
Трьохатомні спирти називають тріолами, або гліцеринами (гліцерилами). Їх назви будують аналогічно до назв двохатомних спиртів, але з додаванням закінчення
-тріол.
Найпростіші представники двох- і трьохатомних спиртів:

Властивості. Хімічні властивості багатоатомних спиртів багато в чому подібні до властивостей одноатомних спиртів. При цьому в реакціях може брати участь як одна, так і дві і більше гідроксильних груп. Нижче розглядаються властивості багатоатомних спиртів на прикладі етиленгліколю і гліцерину. Це безбарвні в`язкі сиропоподібні рідини, солодкуваті на смак, добре розчиняються у воді.
1. Взаємодія з лужними металами. Лужні метали витісняють водень з гідроксильних груп з утворенням гліколятів або гліцератів:
2СН2ОН–СН2ОН + Nа ® 2СН2ОН–СН2ОNа + Н2
Моногліколят натрію
СН2ОН–СН2ОН + 2Nа ® 2СН2ОNа–СН2ОNа + Н2.
Дигліколят натрію
Аналогічно реагує з лужними металами гліцерин, при цьому можуть утворюватись моно-, ди- і тригліцерати.
2. Взаємодія з галогеноводнями. Багатоатомні спирти реагують з галогеноводнями (НСl, НВr, НІ) з утворенням галогенозаміщених спиртів або галогенопохідних алканів:
СН2ОН–СН2ОН + НВr ® СН2ОН–СН2Вr + Н2О
2 Брометанол
або СН2ОН–СН2ОН + 2НВr ® СН2Вr–СН2Вr + Н2О
1,2-Диброметан
3. Взаємодія з кислотами. З кислотами багатоатомні спирти утворюють складні ефіри (естери), наприклад:
СН2ОН–СНОН–СН2ОН + 3НNО3® СН2ОNО2–СНОNО2–СН2ОNО2 + 3Н2О
Гліцерин Нітрогліцерин
Складні ефіри гліцерину з органічними кислотами називають жирами.
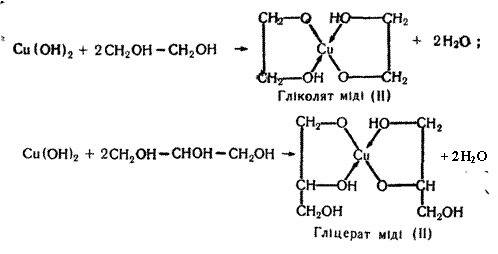 4. Взаємодія з Купрум (II) гідроксидом. Ця реакція характерна тільки для багатоатомних спиртів. Осад Купрум (II) гідроксиду розчиняється в етиленгліколі та гліцерині з утворенням розчину яскраво-синього кольору:
4. Взаємодія з Купрум (II) гідроксидом. Ця реакція характерна тільки для багатоатомних спиртів. Осад Купрум (II) гідроксиду розчиняється в етиленгліколі та гліцерині з утворенням розчину яскраво-синього кольору:
У записаних формулах гліколяту і гліцерату міді (II) стрілками показані донорно-акцепторні зв`язки (Сu – акцептор). Сполуки такого типу належать до комплексних.
Добування і застосування етиленгліколю і гліцерину. Етиленгліколь добувають у промисловості гідратацією (приєднання води) етиленоксиду:
Н2С–СН2 + Н2О ® СН2ОН–СН2ОН.
\ /
О
Етиленоксид
Як і одноатомні спирти, етиленгліколь можна добути гідролізом галогенопохідних алканів водним розчином лугів. Для цієї реакції необхідні
1,2-дигалогенопохідні етану:
СН2Сl–СН2Сl + 2Н2О ® СН2ОН–СН2ОН + 2НСl.
1,2-Дихлоретан
Етиленгліколь утворюється під час пропускання етилену крізь розчин перманганату калію, при цьому відбуваються окислення і гідратація етилену:
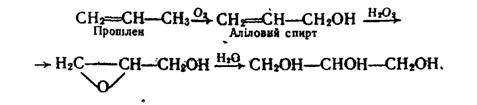 |
СН2=СН2 + [О] + Н2О ® СН2ОН–СН2ОН.
Гліцерин добувають синтетично з пропілену за такою схемою:
Гліцерин входить до складу природних сполук – жирів рослинного і тваринного походження– і може бути виділений з них.
Етиленгліколь і гліцерин використовуються в промисловому органічному синтезі.
Гліцерин застосовують для виробництва мастил, як зм`якшувач шкіри і тканин, у парфюмерній, фармацевтичній і харчовій промисловості.
Водні розчини етиленгліколю і гліцерину замерзають при низьких температурах, тому їх використовують як антифризи – рідини з низькою температурою замерзання, які застосовуються для охолодження двигунів внутрішнього згоряння.