261. Техноекологія
3. Вивчення іонообмінного способу очищення стічних вод
Автор: Міронова Н.Г.
| • 1 |
| Иллюстрация к шагу | 0261-03-001.mp4 |
| Текст к ситуации | Вступ.
Шановний студенте, перед початком виконання лабораторної роботи Вам необхідно ознайомитись із теоретичними відомостями та пройти допуск (тестовий контроль). У разі не проходження тестового контролю Вам потрібно повторно ознайомитись із теоретичним матеріалом та отримати допуск. Після виконання лабораторної роботи Вам необхідно оформити згідно заданої форми звіт та відправити його викладачу. Бажаємо успіхів у виконанні роботи. |
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 2 |
| Текст к ситуации | Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. Порядок виконання роботи Виконання роботи полягає в проведенні очищення стічної води від катіонів міді Cu2+ іонообмінним методом і визначенні ефективності даного методу. Робота складається з декількох стадій. Перша стадія – побудова калібрувального графіка для визначення концентрації іонів міді на фотоелектроколориметрі (ФЕК). Друга – визначення початкової концентрації катіонів міді у стічній воді. Третя – проведення очистки стічної води в іонообмінні колонці. Четверта – визначення кінцевої концентрації катіонів міді у стічній воді та розрахунок ефективності очистки. Побудова калібрувального графіка Готуємо р-н CuSO4∙5H2O з концентрацією 0,1 моль/дм3. Для цього визначаємо молекулярну масу CuSO4∙5H2O за таблицею Менделєєва – Mr(CuSO4∙5H2O) = 63,5 + 32 + 16 ∙ 4 + 5(2∙1 + 16) = 249,5 г/моль. За пропорцією розраховуємо кількість речовини, необхідної для приготування 0,1 молярного розчину: 1М – 249,5 г/моль; 0,1М – Х г/моль. Х = 0,1 ∙ 249,5 / 1 = 24,95 г/моль На технічних терезах зважуємо наважку CuSO4∙5H2O масою 24,95 г і переносимо у мірну колбу місткістю 1 дм3. Поступово додаємо дистильовану воду і ретельно перемішуємо до розчинення речовини. Після цього об’єм розчину доводимо водою до мітки і ретельно перемішуємо. З цього розчину для побудови калібрувального графіка готуємо серію з п’яти розчинів з відомою концентрацією шляхом розведення. Для цього у мірні колби на 25 см3 вносимо такі об’єми вихідного розчину CuSO4∙5H2O, концентрація якого складає 0,1 моль/дм3: V1 = 2,5 см3; V2 = 5 см3, V3 = 12,5 см3, V4 = 17,5 см3, V5 = 20 см3. Доводимо дистильованою водою об’єм колб до мітки. Розраховуємо концентрацію (C2і) кожного з п’яти отриманих розчинів за формулою: С1V1=C2V2, де С1= 0,1 – концентрація вихідного розчину CuSO4∙5H2O, V1і – об’єм 0,1 М р-ну CuSO4∙5H2O, який було взято при приготуванні кожного з п’яти розчинів; V2 = 25 см3 – об’єм колб, у яких готували розчини розведення. Потім на ФЕК вимірюємо оптичну густину кожного отриманого розчину розведення. Для цього наливаємо розчин у кювету, тримаючи її за ребра і слідкуючи за тим, щоб на її поверхні не лишалось крапель води чи розчину або відбитків пальців, оскільки це буде формувати похибку вимірювання. Вставляємо кювету у вимірювальне гніздо. У гніздо порівняння встановлюємо таку ж кювету, заповнену дистильованою водою. Виставляємо світлофільтр та довжину хвилі. Ручка повинна знаходитись у положенні «вліво». Виставляємо прилад на «ноль», повертаючи маховики «грубо» і «точно» таким чином, щоб стрілка прийняла положення по шкалі на позначці «0». Далі переводимо ручку в положення «вправо» і визначаємо по шкалі оптичної густини значення, біля якого зупинилась стрілка. Воно і буде відповідати значенню оптичної густини розчину. Процедуру повторюємо для всіх зразків. Визначення потрібно проводити у порядку збільшення концентрації зразків – від першого до п’ятого. Будуємо графічну залежність оптичної густини (Dі) розчину від його концентрації (C2і). Для цього будуємо координатну площину, де вісь Х – це концентрація розчинів, вісь Y – оптична густина. Відкладаємо п’ять точок з координатами (C2і; Dі) та з’єднуємо їх у графік прямолінійної залежності оптичної густини від концентрації. Визначення початкової концентрації катіонів міді у стічній воді. Вимірюємо оптичну густину розчину до очистки на фотоелектроколориметрі при довжині хвилі λ = 670, чутливостість – 2. Використовуючи калібрувальний графік визначаємо початкову концентрацію у стічній воді. Для цього з точки по вісі Y (значення Dі), яка відповідає виміряній оптичній густині стічної води, проводимо лінію, паралельну вісі Х, до перетину з прямою графіка. З точки перетину опускаємо перпендикуляр на вісь Х і визначаємо концентрацію (Сп). Проведення очистки стічної води в іонообмінні колонці. Збираємо іонообмінну установку, заповнюємо її катіонітом універсальним КУ-2-8 невеликими порціями до потрібного об’єму. Поступово заливаємо 300 см3 стічної води в іонообмінну колонку. Час перебування розчину у катіонообмінній установці 10 хв. Далі відбираємо порцію очищеної води. Визначення кінцевої концентрації катіонів міді у стічній воді та розрахунок ефективності очистки. Вимірюємо оптичну густину розчину на фотоелектроколориметрі при вищевказаних параметрах. Використовуючи калібрувальний графік визначаємо концентрацію очищених стоків (Ск). За визначеними концентраціями до очистки і після очистки розраховуємо ефективність очистки за формулою:
|
| 1 | Продовжити виконання лабораторної роботи | 3 |
| • 3 |
| Текст к ситуации | Готовність до тестування
Пане студенте, для подальшого виконання віртуальної лабораторної роботи необхідно отримати допуск до практичних дій. Для цього необхідно відповісти на питання контролю теоретичних знань, які вимагаються для виконання лабораторної роботи. Якщо Ви впевнені у своїх знаннях та готові відповідати на тестові запитання оберіть пункт – «Матеріал засвоєний», якщо Ви потребуєте додаткового вивчення теоретичного матеріалу оберіть пункт – «Матеріал незасвоєний, потребує повторення». |
| 1 | Матеріал засвоєний | 4 |
| 2 | Матеріал незасвоєний, потребує повторення | 2 |
| • 4 |
| Текст к ситуации | Початок тестування.
При проходженні тестового контролю необхідно звернути увагу на таке: 1. На відповіді виділений обмежений термін. Час, який залишився до закінчення тестування, висвітлюється у верхньому лівому куті екрана монітора комп’ютера. Якщо Ви не надали відповіді у контрольний термін, то відповідь не зараховується. 2. Серед запропонованих відповідей тільки один варіант вірний. |
| 1 | Продовжити виконання лабораторної роботи | 5, 6, 7, 8 |
| • 5 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Метод іонного обміну представляє собою взаємодію |
| 1 | іонів розчину з твердою фазою | 9, 10, 11, 12 |
| 2 | іонів розчину з рідкою фазою | 25 |
| 3 | іонів розчину з газоподібною фозаю | 25 |
| • 6 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Нерозчинні сполуки, які містять у своєму складі функціональні групи, які здатні до обміну з електролітами, - це |
| 1 | іоніти | 9, 10, 11, 12 |
| 2 | адсорбенти | 25 |
| 3 | флокулянти | 25 |
| • 7 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Глинисті мінерали (алюмосилікати), польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу представляють собою |
| 1 | неорганічні природні іоніти | 9, 10, 11, 12 |
| 2 | органічні природні іоніти | 25 |
| 3 | неорганічні синтетичні іоніти | 25 |
| • 8 |
| Ограничение времени | 1 минут |
| Текст к ситуации | синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, нікелю) представляють собою |
| 1 | неорганічні штучні іоніти | 9, 10, 11, 12 |
| 2 | неорганічні природні іоніти | 25 |
| 3 | органічні синтетичні іоніти | 25 |
| • 9 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Кам’яне вугілля, буре вугілля, торф, целюлоза представляють собою |
| 1 | неорганічні штучні іоніти | 25 |
| 2 | органічні штучні іоніти | 25 |
| 3 | органічні природні іоніти | 13, 14, 15, 16 |
| • 10 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Високомолекулярні органічні сполуки - це |
| 1 | органічні синтетичні іоніти | 13, 14, 15, 16 |
| 2 | органічні природні іоніти | 25 |
| 3 | неорганічін природні іоніти | 25 |
| • 11 |
| Ограничение времени | 1 минут |
| Текст к ситуации | За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на такі групи: |
| 1 | порошкоподібні, зернисті, гранульовані, формовані, волокнисті | 13, 14, 15, 16 |
| 2 | пресовані, окатиші, борошноподібні | 25 |
| 3 | крупно-, середньо- та дрібнодисперсні | 25 |
| • 12 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Іоніти, що здатні до обміну катіонів, - це |
| 1 | катіоніти | 13, 14, 15, 16 |
| 2 | аніоніти | 25 |
| 3 | амфоліти | 25 |
| • 13 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Іоніти, що здатні до обміну аніонів, - це |
| 1 | катіоніти | 25 |
| 2 | аніоніти | 17, 18, 19, 20 |
| 3 | амфоліти | 25 |
| • 14 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Іоніти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів |
| 1 | катіоніти | 25 |
| 2 | аніоніти | 25 |
| 3 | амфоліти | 17, 18, 19, 20 |
| • 15 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Залежно від типу протиіонів __________ можуть бути у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах - виберіть пропущене слово |
| 1 | катіоніти | 17, 18, 19, 20 |
| 2 | аніоніти | 25 |
| 3 | амфоліти | 25 |
| • 16 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Залежно від типу протиіонів __________ можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах - виберіть пропущене слово |
| 1 | катіоніти | 25 |
| 2 | аніоніти | 17, 18, 19, 20 |
| 3 | амфоліти | 25 |
| • 17 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Залежно від типу протиіонів __________ можуть бути у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах - виберіть пропущене слово |
| 1 | катіоніти | 25 |
| 2 | аніоніти | 25 |
| 3 | амфоліти | 21, 22, 23, 24 |
| • 18 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Виберіть марку катіоніту сильнокислотного |
| 1 | КУ | 21, 22, 23, 24 |
| 2 | КБ | 25 |
| 3 | КФ | 25 |
| • 19 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Виберіть марку катіоніту слабкокислотного |
| 1 | КУ | 25 |
| 2 | КБ | 21, 22, 23, 24 |
| 3 | КФ | 25 |
| • 20 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Виберіть марку аніоніту високоосновного |
| 1 | АВ | 21, 22, 23, 24 |
| 2 | АН | 25 |
| 3 | АНКБ | 25 |
| • 21 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Виберіть марку аніоніту слабкоосновного |
| 1 | АВ | 25 |
| 2 | АН | 26 |
| 3 | АНКБ | 25 |
| • 22 |
| Ограничение времени | 1 минут |
| Текст к ситуации | Виберіть марку поліамфоліту |
| 1 | КБ | 25 |
| 2 | КФ | 25 |
| 3 | АНКФ | 26 |
| • 23 |
| Ограничение времени | 1 минут |
| Текст к ситуации | С1V1=C2V2 – вказана формула використовується для розрахунку |
| 1 | ефективності очистки стічних вод | 25 |
| 2 | концентрацій у розчинах серії розведення | 26 |
| 3 | об’ємів стічних вод | 25 |
| • 24 |
| Ограничение времени | 1 минут |
| Иллюстрация к шагу | 0261-03-024-00.gif |
| Текст к ситуации | - вказана формула використовується для розрахунку |
| 1 | ефективності очистки стічних вод | 26 |
| 2 | концентрацій у розчинах серії розведення | 25 |
| 3 | об’ємів стічних вод | 25 |
| • 25 |
| Текст к ситуации | Помилка тесту.
На жаль, Ви неправильно відповіли на питання тесту, тому пропонуємо Вам уважно переглянути теоретичний матеріал і після цього спробувати повторно надати відповіді на питання тестового контролю. |
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 26 |
| Текст к ситуации | Завершення тестування.
Вітаємо, Ви правильно відповіли на питання тестового контролю знань та умінь теоретичного матеріалу, необхідного для проведення лабораторної роботи. Бажаємо Вам успішного виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 27 |
| • 27 |
| Текст к ситуации | Тема: Вивчення іонообмінного способу очищення стічних вод.
Мета: Вилучення іонів важких металів із стічних вод за допомогою катіонітового фільтру . |
| 1 | Продовжити виконання лабораторної роботи | 28 |
| • 28 |
| Иллюстрация к шагу | 0261-03-028.mp4 |
| Текст к ситуации | Матеріали, реактиви, устаткування:
1 Катіонова колонка; 2 Терези; 3 Фотоелектроколориметр (ФЕК); 4 Піпетки; 5 Мірні колби місткістю 25 см3 та 1 дм3; 6 Хімічні склянки місткістю 200-400 см3; 7 Катіоніт марки КУ-2-8. |
| 1 | Продовжити виконання лабораторної роботи | 29 |
| • 29 |
| Текст к ситуации | Побудова калібрувального графіка. |
| 1 | Продовжити виконання лабораторної роботи | 30 |
| • 30 |
| Текст к ситуации | Приготування вихідного розчину концентрацією 0,1 моль/л.
Для цього визначаємо молекулярну масу CuSO4 ∙ 5H2O за таблицею Менделєєва – Mr(CuSO4 ∙ 5H2O) = 63,5 + 32 + 16 ∙ 4 + 5(2 ∙ 1 + 16) = 249,5 г/моль. За пропорцією розраховуємо кількість речовини, необхідної для приготування 0,1 молярного розчину: 1М – 249,5 г/моль; 0,1М – Х г/моль. Х = 0,1 ∙ 249,5 / 1 = 24,95 г/моль |
| 1 | Продовжити виконання лабораторної роботи | 31 |
| • 31 |
| Иллюстрация к шагу | 0261-03-031.mp4 |
| Текст к ситуации | Зважуємо наважку CuSO4 ∙ 5H2O в кількості 24,95 г. |
| 1 | Продовжити виконання лабораторної роботи | 32 |
| • 32 |
| Иллюстрация к шагу | 0261-03-032.mp4 |
| Текст к ситуации | Переносимо наважку у мірну колбу місткістю 1 дм3. Поступово додаємо дистильовану воду і ретельно перемішуємо до розчинення наважки. Після цього об’єм розчину доводимо водою до мітки і ретельно перемішуємо. |
| 1 | Продовжити виконання лабораторної роботи | 33 |
| • 33 |
| Иллюстрация к шагу | 0261-03-033.mp4 |
| Текст к ситуации | З цього розчину для побудови калібрувального графіка готуємо серію з п’яти розчинів з відомою концентрацією шляхом розведення. Для цього у мірні колби на 25 см3 вносимо такі об’єми вихідного розчину CuSO4 ∙ 5H2O, концентрація якого складає 0,1 моль/л: V1 = 2,5 см3; V2 = 5 см3, V3 = 12,5 см3, V4 = 17,5 см3, V5 = 20 см3. Доводимо дистильованою водою об’єм колб до мітки. |
| 1 | Продовжити виконання лабораторної роботи | 34 |
| • 34 |
| Текст к ситуации | Розраховуємо концентрацію (C2і) кожного з п’яти отриманих розчинів за формулою:
С1V1і=C2іV2, де С1= 0,1 – концентрація вихідного розчину CuSO4 ∙ 5H2O, V1і – об’єм 0,1 М р-ну CuSO4 ∙ 5H2O, який було взяти при приготуванні кожного з п’яти розчинів; V2 = 25 см3 – об’єм колб, у яких готували розчини розведення. |
| 1 | Продовжити виконання лабораторної роботи | 35 |
| • 35 |
| Текст к ситуации | Розрахункова концентрація 1-го розчину дорівнює, моль/л, (оберіть правильну відповідь): |
| 1 | C21=0,01 | 36 |
| 2 | C21=0,015 | 57 |
| • 36 |
| Текст к ситуации | Розрахункова концентрація 2-го розчину дорівнює, моль/л, (оберіть правильну відповідь): |
| 1 | C22=0,02 | 37 |
| 2 | C22=0,20 | 58 |
| • 37 |
| Текст к ситуации | Розрахункова концентрація 3-го розчину дорівнює, моль/л, (оберіть правильну відповідь): |
| 1 | C23=0,05 | 38 |
| 2 | C23=0,06 | 59 |
| • 38 |
| Текст к ситуации | Розрахункова концентрація 4-го розчину дорівнює, моль/л, (оберіть правильну відповідь): |
| 1 | C24=0,07 | 39 |
| 2 | C24=0,017 | 60 |
| • 39 |
| Текст к ситуации | Розрахункова концентрація 5-го розчину дорівнює, моль/л, (оберіть правильну відповідь): |
| 1 | C25=0,08 | 40 |
| 2 | C25=0,008 | 61 |
| • 40 |
| Иллюстрация к шагу | 0261-03-040.mp4 |
| Текст к ситуации | Підготовка фотоелектроколориметра (ФЕК) до вимірювання.
Включити прибор. Прогріти його протягом 30 хв. Виставити довжину хвилі λ = 670, чутливість – 2. Наливаємо дистильовану воду у кювету до мітки та вставляємо її у гніздо порівняння. У положенні ручки «вліво» виставляємо шкалу оптичної густини на «ноль», користуючись маховиками «грубо», «точно». Наливати рідину в кювету потрібно обережно, тримаючи кювету за ребра і слідкуючи за тим, щоб на її поверхні не лишалось крапель води чи розчину або відбитків пальців, оскільки це буде формувати похибку вимірювання. |
| 1 | Продовжити виконання лабораторної роботи | 41 |
| • 41 |
| Иллюстрация к шагу | 0261-03-041.mp4 |
| Текст к ситуации | Вимірювання оптичної густини 1-го розчину.
Наливаємо в кювету 1-ий розчин. Вставляємо її в гніздо. Переводимо ручку з положення «вліво» в положення «вправо» і визначаємо оптичну густину по шкалі, звертаючи увагу на ціну поділки. Визначення проводиться тричі. Після вимірювання розчин виливають. Кювету промивають спочатку дистильованою водою, а потім наступним розчином, який буде вимірюватись. Оптична густина 1-го розчину дорівнює (виберіть значення, що відповідає зображенню). |
| 1 | D1 = 0,06 | 42 |
| 2 | D1 = 0,08 | 62 |
| • 42 |
| Иллюстрация к шагу | 0261-03-042.mp4 |
| Текст к ситуации | Вимірювання оптичної густини 2-го розчину.
Наливаємо в кювету 2-ий розчин. Вставляємо її в гніздо. Переводимо ручку з положення «вліво» в положення «вправо» і визначаємо оптичну густину по шкалі, звертаючи увагу на ціну поділки. Визначення проводиться тричі. Після вимірювання розчин виливають. Кювету промивають спочатку дистильованою водою, а потім наступним розчином, який буде вимірюватись. Оптична густина 2-го розчину дорівнює (виберіть значення, що відповідає зображенню). |
| 1 | D2 = 0,08 | 43 |
| 2 | D2 = 0,082 | 63 |
| • 43 |
| Иллюстрация к шагу | 0261-03-043.mp4 |
| Текст к ситуации | Вимірювання оптичної густини 3-го розчину.
Наливаємо в кювету 3-ий розчин. Вставляємо її в гніздо. Переводимо ручку з положення «вліво» в положення «вправо» і визначаємо оптичну густину по шкалі, звертаючи увагу на ціну поділки. Визначення проводиться тричі. Після вимірювання розчин виливають. Кювету промивають спочатку дистильованою водою, а потім наступним розчином, який буде вимірюватись. Оптична густина 3-го розчину дорівнює (виберіть значення, що відповідає зображенню). |
| 1 | D3 = 0,24 | 44 |
| 2 | D3 = 0,186 | 64 |
| • 44 |
| Иллюстрация к шагу | 0261-03-044.mp4 |
| Текст к ситуации | Вимірювання оптичної густини 4-го розчину.
Наливаємо в кювету 4-ий розчин. Вставляємо її в гніздо. Переводимо ручку з положення «вліво» в положення «вправо» і визначаємо оптичну густину по шкалі, звертаючи увагу на ціну поділки. Визначення проводиться тричі. Після вимірювання розчин виливають. Кювету промивають спочатку дистильованою водою, а потім наступним розчином, який буде вимірюватись. Оптична густина 4-го розчину дорівнює (виберіть значення, що відповідає зображенню). |
| 1 | D4 = 0,33 | 45 |
| 2 | D4 = 0,255 | 65 |
| • 45 |
| Иллюстрация к шагу | 0261-03-045.mp4 |
| Текст к ситуации | Вимірювання оптичної густини 5-го розчину.
Наливаємо в кювету 5-ий розчин. Вставляємо її в гніздо. Переводимо ручку з положення «вліво» в положення «вправо» і визначаємо оптичну густину по шкалі, звертаючи увагу на ціну поділки. Визначення проводиться тричі. Після вимірювання розчин виливають. Кювету промивають спочатку дистильованою водою, а потім наступним розчином, який буде вимірюватись. Оптична густина 5-го розчину дорівнює (виберіть значення, що відповідає зображенню). |
| 1 | D5 = 0,36 | 46 |
| 2 | D5 = 0,29 | 66 |
| • 46 |
| Иллюстрация к шагу | 0261-03-046-00.gif |
| Текст к ситуации | Будуємо графічну залежність оптичної густини (Dі) розчину від його концентрації (C2і). Для цього будуємо координатну площину, де вісь Х – це концентрація, вісь Y – оптична густина. Відкладаємо п’ять точок з координатами (C2і; Dі) та з’єднуємо їх у графік прямолінійної залежності оптичної густини від концентрації. |
| 1 | Продовжити виконання лабораторної роботи | 47 |
| • 47 |
| Иллюстрация к шагу | 0261-03-047.mp4 |
| Текст к ситуации | Визначення концентрації стічної води до очистки.
Наливаємо в кювету стічну воду до очистки. Вставляємо кювету в гніздо. Переводимо ручку з положення «вліво» в положення «вправо» і визначаємо оптичну густину по шкалі, звертаючи увагу на ціну поділки. Визначення проводиться тричі. Після вимірювання розчин виливають. Кювету промивають спочатку дистильованою водою, а потім наступним розчином, який буде вимірюватись. |
| 1 | Продовжити виконання лабораторної роботи | 48 |
| • 48 |
| Иллюстрация к шагу | 0261-03-048.mp4 |
| Текст к ситуации | Оптична густина стічної води до очистки дорівнює (виберіть значення, що відповідає зображенню). |
| 1 | Дпоч.=0,21 | 49 |
| 2 | Дпоч.=0,188 | 67 |
| • 49 |
| Иллюстрация к шагу | 0261-03-049-00.gif |
| Текст к ситуации | Використовуючи калібрувальний графік визначаємо початкову концентрацію у стічній воді. Для цього з точки по вісі Y (значення Dі), яка відповідає виміряній оптичній густині стічної води, проводимо лінію, паралельну вісі Х, до перетину з прямою графіка. З точки перетину опускаємо перпендикуляр на вісь Х і визначаємо концентрацію (Сп). |
| 1 | Продовжити виконання лабораторної роботи | 50 |
| • 50 |
| Иллюстрация к шагу | 0261-03-050.mp4 |
| Текст к ситуации | Підготовка установки іонообмінної очистки до роботи.
Збираємо іонообмінну установку, заповнюємо її катіонітом універсальним КУ-2-8 невеликими порціями до потрібного об’єму. Поступово заливаємо 300 см3 стічної води в іонообмінну колонку. Час перебування розчину у катіонообмінній установці 10 хв. |
| 1 | Продовжити виконання лабораторної роботи | 51 |
| • 51 |
| Иллюстрация к шагу | 0261-03-051.mp4 |
| Текст к ситуации | Проводимо вимірювання концентрації стічної води після очистки.
Відбираємо порцію очищеної води. Наливаємо в кювету очищену стічну воду. Вставляємо кювету в гніздо. Переводимо ручку з положення «вліво» в положення «вправо» і визначаємо оптичну густину по шкалі, звертаючи увагу на ціну поділки. Визначення проводиться тричі. Після вимірювання розчин виливають. Кювету промивають дистильованою водою. |
| 1 | Продовжити виконання лабораторної роботи | 52 |
| • 52 |
| Иллюстрация к шагу | 0261-03-052.mp4 |
| Текст к ситуации | Оптична густина стічної води після очистки дорівнює (виберіть значення, що відповідає зображенню). |
| 1 | Дкін.=0,025 | 53 |
| 2 | Дкін.=0,109 | 68 |
| • 53 |
| Текст к ситуации | Використовуючи калібрувальний графік визначаємо кінцеву концентрацію у стічній воді (Скін.). |
| 1 | Продовжити виконання лабораторної роботи | 54 |
| • 54 |
| Текст к ситуации | За визначеними концентраціями розраховуємо ефективність іонообмінної очистки по катіону міді (ŋ, %) очистки згідно формули:
ŋ=(Cпоч. - Cкін.) ∙ 100 / Cпоч. |
| 1 | ŋ=89 % | 55 |
| 2 | ŋ=99 % | 40 |
| • 55 |
| Текст к ситуации | Вітаємо! Ви успішно виконали лабораторну роботу.
Тепер оформіть звіт з лабораторної роботи згідно представленого зразка, запишіть його окремим файлом та і відправте викладачу зі своєї персональної сторінки. |
| 1 | Продовжити виконання лабораторної роботи | 56 |
| • 56 |
| Текст к ситуации | Оформіть протокол та видішліть його викладачу.
Лабораторна робота №1 Тема роботи. Вивчення іонообмінного способу очищення стічних вод. Мета роботи: вилучення іонів двох-, трьохвалентних металів за допомогою катіонітового фільтра. Матеріали, реактиви, устаткування: катіонітова колона, технічні терези, ФЕК, мірні колби місткістю 25 см3 та 1 дм3, піпетки, хімічні склянки місткістю 200 – 400 см3, катіоніт марки КУ-2-8. Обробка результатів 1. Результати для побудови калібрувального графіка занести в таблицю 1. Таблиця 1 – Значення концентрацій розчинів і їхніх оптичних густин для побудови каліброваного графіка
2. Побудувати калібрувальний графік, за отриманими Вами в процесі виконання роботи точками. 3. За визначеними концентраціями катіонів міді у стічній воді до очистки і після розрахувати ефективність очистки, використовуючи формулу:
4. Результати проведення іонообмінної очистки стічної води занести в таблицю 2. Таблиця 2 – Результати проведення очистки стічної води
5. Зробити висновок про ефективність методу для даного забруднювача. |
| • 57 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 35 |
| • 58 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 36 |
| • 59 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 37 |
| • 60 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 38 |
| • 61 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 39 |
| • 62 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 41 |
| • 63 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 42 |
| • 64 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 43 |
| • 65 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 44 |
| • 66 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 45 |
| • 67 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 48 |
| • 68 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей крок лабораторної роботи. Теоретичні відомості Одним із типових процесів технології водоочищення і водопідготовки є іонний обмін, який здійснюється із застосуванням іонообмінних матеріалів (іонітів). Метод іонного обміну представляє собою взаємодію розчину з твердою фазою-іонітом, що має властивості обмінювати іони, які містяться в ньому, на іоні, що знаходяться у водному розчині. Іоніти – це нерозчинні сполуки, які містять у своєму складі функціональні групи, здатні до іонізації та обміну з електролітами. Багато іонітів існують у природному вигляді (цеоліт, алюмосилікат) та більшу частину їх отримують синтетичним шляхом. За природою іоніти поділяють на неорганічні (мінеральні) і органічні, природні і штучні (синтетичні). До неорганічних природних іонітів належать природні цеоліти, глинисті мінерали (алюмосилікати), в тому числі бентонітові глини, глауконіт, вермикуліт, польові шпати, фельдшпатоїди, слюди, оксиди, фосфати і силікати металів (титану, кальцію, цирконію та ін.), рудні мінерали змінного складу. До неорганічних штучних іонітів відносять синтетичні цеоліти, важкорозчинні солі гетерополікислот, фероціаніди, фосфати, гідрооксиди, оксиди, сульфіди металів (цирконію, алюмінію, феруми, титану, ніколу та ін.). До органічних природних іонообмінних матеріалів належать кам’яне вугілля і буре вугілля, торф, целюлоза. Синтетичні органічні іоніти є високомолекулярними органічними сполуками, які спрямовано синтезовані, мають сталий склад і властивості, що відтворюються в результаті різних технологічних операцій. Для них характерна висока здатність до обміну іонами, хімічна стійкість і механічна міцність. Синтетичні іоніти знайшли найбільш широке застосування в технології водопідготовки і водоочищення. За зовнішнім виглядом і ступенем дисперсності іоніти поділяють на порошкоподібні, зернисті, гранульовані, формовані і волокнисті. За типом і знаком протиіонів іоніти поділяють на: а) катіоніти, що здатні до обміну катіонів; б) аніоніти, що здатні до обміну аніонів; в) амфоліти, що здатні залежно від умов середовища до обміну як катіонів, так і аніонів. Катіоніти залежно від типу протиіонів можуть перебувати у водневій (Н-формі), сольовій ( натрієвій, кальцієвій, тощо) і змішаній формах. Аніоніти можуть бути в гідроксидній (ОН-формі), сольовій (хлоридній, сульфатній тощо) і змішаній формах. Амфоліти бувають у воднево-гідроксильній, воднево-сольовій, гідроксильно-сольовій і сольовій формах. Іоніти, маркують так КУ (катіоніт універсальний) – сильнокислотний катіоніт; КБ (катіоніт буферний) – слабкокислотний катіоніт; КФ – катіоніт фосфатний; АВ – аніоніт високоосновний; АН – аніоніт слабкоосновний; АНКБ – аніоніт слабкоосновний, катіоніт буферний (поліамфоліт), який містить слабкоосновні і слабкокислотні групи; АНКФ – поліамфоліт, який містить слабкоосновні і фосфатні групи і тощо. Для завантаження Н-катіонітових фільтрів при очищенні стічних вод на даний час переважно використовують катіоніти КУ-1, КУ-2-8, КУ-2-20, КУ-23, КБ-4, КБ-4П-2, КБ-4-10П. В якості слабо основних аніонітів можуть використовуватися: АН-2-ФН, АН-18, АН-22, АН-32, АН-221, АН-251, сильно основні аніоніти АВ-17-8, АВ-29-12П. Регенерація іонообмінних смол полягає у відновленні початкової іонної форми смоли. |
| 1 | Продовжити виконання лабораторної роботи | 52 |
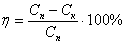 .
.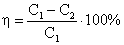 ;
;