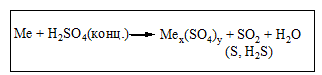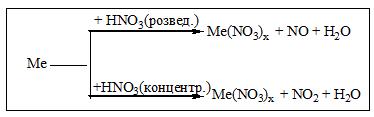194. Хімія
1. Класи неорганiчних сполук
Автор: Хрящевський В.М.
| • 1 |
| Иллюстрация к шагу | 0194-01-001.mp4 |
| Текст к ситуации | ЛАБОРАТОРНІ РОБОТИ з курсу "Хімія" для студентів нехімічних спеціальностей ЗАГАЛЬНІ ВКАЗІВКИ Виконання лабораторних робіт є невід’ємною частиною вивчення курсу хімії для студентів будь-якої спеціальності, тому що, за словами М.В.Ломо-носова, "…химию нико-им образом понять невозможно, не познав самой практики, не проделав самостоятельных опытов…" Звичайно, ніякі віртуальні досліди не можуть замінити реальної роботи з справжніми реактивами, але, на наше сподівання, вони все ж таки дадуть можливість ознайомитися з основними прийомами роботи в хімічній лабораторії, опрацювати методику постановки хімічного експерименту, його виконання та осмислення. Виконання лабораторної роботи починається з уважного опрацювання теоретичного матеріалу теми, короткий зміст якого наведено перед завданнями до роботи. Не познайомившись з цим матеріалом, студент не зможе вірно осмислити суть хімічного експерименту, описати його та зробити висновки. Тому перед безпосереднім виконанням роботи студент повинен відповісти на ряд запитань, які мають за мету перевірити ступінь засвоєння теми, і при достатньому рівні засвоєння одержати дозвіл на виконання роботи. Після того, як всі досліди лабораторної роботи будуть виконані, зафіксовані і ос-мислені, студент повинен оформити журнал проведення дослідів, форму якого наведено нижче (на початку експериментальної частини лабораторної роботи) Оформлений лабораторний журнал надсилається викладачу, який перевіряє його, робить зауваження, і зараховує (або не зараховує) лабораторну роботу, про що повідомляє студента. |
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 2 |
| Текст к ситуации | Уважно опрацюйте теоретичний матеріал теми. Не познайомившись з цим матеріалом, Dи не зможете вірно осмислити суть хімічного експерименту, описати його та зробити висновки.
Класифікація і номенклатура неорганічних сполук Речовини
Міжнародна номенклатура IUPAC (Міжнародний союз теоретичної і прикладної хімії) 1. Хімічну формулу складної сполуки умовно поділяють на позитивно заряджену частинку (катіон) і негативну – аніон, позитивна частинка стоїть на першому місці. Сa+2O-2 H2+SO4-2 2. Першим називають катіон, потім аніон – обидва у називному відмінку. Якщо аніон складається з атомів одного елемента, то до його латинської назви додається суфікс –ід (-ид), якщо – з кількох, то суфікс –ат, вказується кількість і латинська назва елементів, в дужках можна вказувати валентність. Числівникові префікси: 1 – моно; 2 – ди; 3 – три; 4 – тетра; 5 – пента; 6 – гекса; 7 – гепта; 8 – окта; 9 – нона. CaO – кальцій оксид H2SO4 – дигідроген тетраоксосульфат, гідроген сульфат (VI) ICl3 – йод трихлорид, йод(ІІІ) хлорид K2S – дикалій сульфід K2Cr2O7 – дикалій гептаоксодихромат Оксиди Оксиди – це бінарні сполуки елементів з оксигеном: - несолетворні (CO, NO, SiO); - солетворні: основні, кислотні, амфотерні. Одержання: 1. Взаємодія з киснем: 2 Cu + O2→(t°) 2 CuO 4 P + 5 O2→(t°) 2 P2O5 2 H2S + 3 O2→ (t°) 2 SO2 + 2 H2O 2. Розклад складних речовин: 2 Fe(OH)3→ (t°) Fe2O3 + 3 H2O H2SO3→ (t°) SO2 + H2O CaCO3→ (t°) CaO + CO2 Класифікація: 1. Основні оксиди – взаємодіють з кислотами з утворенням солей. Основним оксидам відповідають основи. Основні оксиди утворюють: - метали з валентністю В=І: K2O, Cu2O, Ag2O. - більшість металів з В=ІІ: CaO, FeO, CoO, MnO. - деякі метали з В=ІІІ, IV: Tl2O3, Bi2O3, UO2. K2O + H2SO4→ K2SO4 + H2O FeO + 2 HCl → FeCl2 + H2O Na2O + H2O → 2 NaOH (лужні, лужноземельні метали) 2. Кислотні оксиди – взаємодіють з лугами з утворенням солі і води, їм відповідають кислоти. Кислотні оксиди утворюють: - неметали: SO2, P2O5, CO2, Cl2O7. - метали з В=V, VI, VII: V2O5, WO3, Mn2O7. SO2 (H2SO3) + NaOH → Na2SO3 + H2O V2O5 (HVO3) + 2 KOH → 2 KVO3 + H2O N2O3 + H2O →2 HNO2 (більшість кислотних оксидів) 3. Амфотерні оксиди – взаємодіють з кислотами і лугами з утворенням солі і води. Амфотерні оксиди утворюють: - деякі метали з В=ІІ: ZnO, BeO, SnO, PbO, GeO. - більшість металів з В=ІІІ, ІV: Al2O3, In2O3, Co2O3, SnO2, PbO2, MnO2. - деякі метали з В=V, VI: Nb2O5, UO3. Основні властивості: Al2O3 + 3 H2SO4→ Al2(SO4)3 + 3 H2O Кислотні властивості: Сплавлення: Al2O3 (HAlO2) + 2 NaOH→2 NaAlO2 + H2O Водний розчин: Al2O3 + 6 NaOH+ 3 H2O→2 Na3[Al(OH)6] Взаємодія між оксидами з утворенням солей: - основний + кислотний: CaO + SO3→ CaSO4 - основний + амфотерний: K2O + BeO → K2BeO2 - амфотерний + кислотний: BeO + N2O5→Be(NO3)2 Номенклатура: Назви оксидів складаються з назви елемента у називному відмінку і слова „оксид” з використанням числівникових префіксів або вказуючи валентність елемента: N2O5 – динітроген пентаоксид; нітроген (V) оксид Гідроксиди (гідрати оксидів): - основні (основи); - амфотерні (амфоліти); - кислотні (кислоти). Основи Основи – це сполуки, що містять негативно заряджену частинку (аніон) ОН- і катіон металу (NaOH, Cu(OH)2), катіон амоніаку (NH4OH) чи складну групу (ТіО2+: ТіО(ОН)2).
Номенклатура: Назва елемента (його валентність) + слово „гідроксид” Сu(OH)2 – купрум дигідроксид, купрум (ІІ) гідроксид. Амфотерні гідроксиди Амфотерним оксидам відповідають амфотерні гідроксиди (називаються як основи): Zn(OH)2 – цинк гідроксид Sn(OH)2 – станум (ІІ) гідроксид Всі вони нерозчинні у воді, тому їх добувають за реакцією солі з лугом: SnCl2 + 2 KOH→Sn(OH)2 + 2 KCl Взаємодіють з кислотами і лугами: Основні властивості: Sn(OH)2 + 2 HNO3→Sn(NO3)2 + 2 H2O Кислотні властивості: Сплавлення: Sn(OH)2 + 2 NaOH→Na2SnO2 + 2 H2O У водному розчині: Sn(OH)2 + 2 NaOH→Na2[Sn(OH)4] Кислоти Кислоти – це сполуки, що містять гідроген-катіони, які здатні заміщуватися на метал і утворювати при цьому солі, і кислотний залишок. За хімічним складом кислоти поділяють на: - безоксигенові: HCl, HBr, H2S, HCN; - звичайні оксигеновмісні – це гідрати кислотних оксидів: H2SO4 (SO3 + H2O), H3PO4 (P2O5 + H2O); - полікислоти: H2Cr2O7, H4P2O7. - тіокислоти – похідні звичайних оксигеновмісних кислот, в яких один або кілька атомів оксигену заміщені на атом сульфуру: H2SO4→ H2SO3S → H2S2O3 - тіосульфатна кислота - пероксокислоти: один або кілька атомів оксигену заміщені на пероксогрупу –О–О–: H2SO4→H2SO5 - пероксосульфатна кислота За основністю, яка визначається кількістю атомів гідрогену, здатних заміщуватися на метал, кислоти поділяють на: - одноосновні: HCl, HNO3 - двоосновні: H2S, H2CO3 - триосновні: H3PO4, H3PO3 - чотирьохосновні: H4P2O7, H4SiO4 - п’ятиосновні: H5IO6 - шестиосновні: H6TeO6 Одержання кислот: 1. Кислотний оксид + вода: CrO3 + H2O → H2CrO4 CO2 + H2O → H2CO3 2. Сіль більш слабкої кислоти + більш сильна кислота: FeS + 2 HCl → FeCl2 + H2S 2 CH3COONa + H2SO4→2 CH3COOH + Na2SO4 Хімічні властивості кислот: 1. Всі кислоти реагують з речовинами основного характеру (основними і амфотерними оксидами, основами, амфотерними гідроксидами) з утворенням солей: 2 HCl + CuO→CuCl2 + H2O 2 HCl + ZnO→ZnCl2 + H2O 2 HNO3 + Mg(OH)2→ Mg(NO3)2 + 2 H2O 3 HNO3 + Al(OH)3→Al(NO3)3 + 3 H2O 2. Взаємодія металів з найбільш важливими кислотами: А)Метали, що стоять в електрохімічному ряді напруг до Гідрогену витісняють водень Н2 з розчинів кислот: HCl, H2SO4(розв.), H2CO3, H3PO4 (крім HNO3 та конц. H2SO4): Mg + H2SO4→MgSO4 + H2 Cu + H2SO4(розвед.) → не реагує Б) Концентрована H2SO4 та HNO3(розведена та концентрована) реагують з металами, які стоять в ряду напруг від Li до Ag включно. Газ водень при цьому не виділяється!!!Ферум , Хром, Алюміній не реагують з концентрованою HNO3на холоду!!! (пасивація металу). Метали середньої активності та малоактивні метали реагують з цими кислотами за схемами:
При взаємодії нітратної кислоти з металами можуть утворюватись іінші продукти відновлення Нітрогену(+5) :N2, N2O, NH4NO3. Електрохімічний ряд напруг металів
3. Кислоти реагують з солями більш слабких або летких кислот: 2 HCl + Na2CO3→2 NaCl + H2CO3 (CO2 + H2O) Номенклатура кислот Назви кислот утворюють від назви аніонів кислотних залишків з додаванням закінчення „на” та слова „кислота”. 1. Назви безоксигенових кислот. Назва аніона (латинська назва елемента + суфікс –ід (-ид)) + закінчення „на” + слово „кислота”: HCl – хлоридна кислота H2S – сульфідна кислота. 2. Назви оксигеновмісних кислот. 2.1. Назва аніона (латинська назва елеманта + суфікс –ат) + закінчення „на” + слово „кислота”. В дужках вказується валентність кислотоутворюючого елемента. Якщо елемент знаходиться у вищому ступені окиснення, то його валентність і кількість атомів оксигену можна не вказувати: H2Se+4O3 – селенатна (IV) кислота H2Se+6O4 – селенатна (VІ) кислота, селенатна кислота H2Mn+6O4 – манганатна (VI) кислота HSb+5O3 – стибатна (V) кислота, стибатна кислота 2.2. Кислоти можна називати по назвах аніонів з використанням префіксів і суфіксів без вказування валентності. Якщо елемент утворює кислоти в двох ступенях окиснення (+2, +4; +4, +6; +3, +5), то до назви елемента додають суфікс –ат (у вищому ступені окиснення) і –іт(-ит) (у другому ступені окиснення): H2Se+4O3 – селенітна кислота H2Se+6O4 – селенатна кислота HSb+5O3 – стибатна кислота HSb+3O2 – стибітна кислота Якщо елемент утворює кислоти більше ніж в двох ступенях окиснення, то використовують префікси і суфікси (Cl, Br, I, Mn):
Якщо одному елементу з певним ступенем окиснення відповідають кілька кислот, то до назви додають префікс: мета- для кислот з минимальним числом атомів гідрогену орто- для кислот з максимальним числом атомів гідрогену. НР+5О3 – метафосфатна кислота Н3Р+5О4 – ортофосфатна кислота Солі Солі – це кристалічні речовини, що містять катіон металу або NH4 і кислотний залишок. Найпоширеніший спосіб добування – реакція нейтралізації – взаємодія кислоти з основою: кислота (Н+) + основа (ОН-) → сіль + вода Класифікація: 1. Середні (нормальні) солі – утворюються при повному заміщенні атомів гідрогену в кислоті на метал (Na2SO4, K2CO3, CuS): H2SO4 + Mg(OH)2→MgSO4 + 2 H2O Назви середніх солей утворюють з назви катіона метала і аніона кислотного залишку у називному відмінку: MgSO4 – магній сульфат Fe(NO3)3 – ферум (ІІІ) нітрат 2. Кислі солі (гідрогенсолі) – утворюються при неповному заміщенні атомів гідрогену в кислоті на метал: 2 H2SO4 + Mg(OH)2→ Mg(HSO4)2 + 2 H2O надлишок недостача Назви утворюються з назви середньої солі з додаванням до назви аніона слова „гідроген”: Mg(HSO4)2 – магній гідрогенсульфат Ba(H2PO4)2 – барій дигідрогенортофосфат 3. Основні солі (гідроксосолі) – утворюються при неповному заміщенні ОН--груп в основі на кислотні залишки: H2SO4 + 2 Mg(OH)2→(MgОН)2SO4 + 2 H2O недостача надлишок Назви утворюються з назви середньої солі з додаванням до назви катіона слова „гідроксо”: (MgОН)2SO4 – гідроксомагній сульфат Al(OH)2Cl – дигідроксоалюміній хлорид Формули і назви кислот
Технічні і побутові назви деяких речовин Їдкий натр NaOH Мідний купорос CuSO4 · 5 H2O Сода Na2CO3 Натрієва селітра NaNO3 Кристалічна сода Na2CO3 · 10 H2O Вапняк, крейда, мармур CaCO3 Питна сода NaHCO3 Простийсуперфосфат Ca(H2PO4)2+CaSO4 Кухонна сіль NaCl Подвійний суперфосфат Ca(H2PO4)2 Сірчистий ангідрид SO2 Доломіт CaCO3 + MgCO3 Кварц SiO2 Поташ K2CO3 Мінерал корунд Al2O3 (+Cr) – рубін, (+Ti) – сапфір Гашене вапно Ca(OH)2 Малахіт (CaOH)2CO3 Негашене вапно CaO Рідке скло Na2SiO3 Плавікова кислота HF Азбест CaO · 3 MgO · 4 SiO2 Соляна кислота HCl Ціаністий калій KCN Глауберова сіль Na2SO4 · 10 H2O Сурік Pb3O4 (Pb2PbO4) Гірка сіль MgSO4 · 7 H2O Бура Na2B4O7 · 10 H2O Гіпс CaSO4 · 2 H2O Алебастр 2 CaSO4 · H2O | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 3 |
| • 3 |
| Текст к ситуации | УВАГА! Для виконання лабораторної роботи Вам треба відповісти на декіль-ка запитань. Допуск на проведення дослідів Ви одержуєте тільки після вірних відповідей.
Далі Вам буде запропоновано 4 питання. У разі невірної відповіді хоч на одне питання результат не зараховується. Ви знову можете повернутись до теоретичних відомостей і краще підготуватись до тестування. Якщо Ви готові, починайте тесту-вання. Серед запропонованих варіантів відповідей тільки одна правильна. |
| 1 | Продовжити виконання лабораторної роботи | 5, 6, 7 |
| • 4 |
| Текст к ситуации | Помилка тесту.
На жаль, Ви неправильно відповіли на питання тесту, тому пропонуємо Вам уважно перег-лянути теоретичний матеріал і після цього спробувати повторно надати відповіді на питан-ня тестового контролю. |
| 1 | Продовжити виконання лабораторної роботи | 2 |
| • 5 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Вкажіть формулу сульфур(ІV) оксиду |
| 1 | SО3 | 4 |
| 2 | SО | 4 |
| 3 | SО2 | 8, 9, 10 |
| • 6 |
| Ограничение времени | 5 минут |
| Текст к ситуации | До якого типу оксидів належить оксид SО2? |
| 1 | кислотний | 8, 9, 10 |
| 2 | основний | 4 |
| 3 | амфотерний | 4 |
| • 7 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Яка сполука утворюється при взаємодії сульфур(ІV) оксиду з водою? |
| 1 | Н2SО4 | 4 |
| 2 | Н2SО2 | 4 |
| 3 | Н2SО3 | 8, 9, 10 |
| • 8 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Вкажіть формулу магній оксиду |
| 1 | МgО2 | 4 |
| 2 | МgО | 11, 12, 13 |
| 3 | Мg2О | 4 |
| • 9 |
| Ограничение времени | 5 минут |
| Текст к ситуации | До якого типу оксидів належить оксид МgО? |
| 1 | кислотний | 4 |
| 2 | основний | 11, 12, 13 |
| 3 | амфотерний | 4 |
| • 10 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Яка сполука утворюється при взаємодії магній оксиду з водою? |
| 1 | Мg(ОН)2 | 11, 12, 13 |
| 2 | Мg(ОН)3 | 4 |
| 3 | МgОН | 4 |
| • 11 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Який з вказаних гідроксидів належить до основних? |
| 1 | Zn(ОН)2 | 4 |
| 2 | Nі(ОН)2 | 14, 15, 16 |
| 3 | Сr(ОН)3 | 4 |
| • 12 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Які з вказаних гідроксидів реагують з лугом? |
| 1 | Zn(ОН)2 тa Сr(ОН)3 | 14, 15, 16 |
| 2 | Zn(ОН)2 та Nі(ОН)2 | 4 |
| 3 | тільки Сr(ОН)3 | 4 |
| • 13 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Вкажіть продукт взаємодії хром(ІІІ) гідроксиду з розчином лугу |
| 1 | Сr(ОН)3 | 4 |
| 2 | Nа[Сr(ОН)4] | 14, 15, 16 |
| 3 | Nа2СrО4 | 4 |
| • 14 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Вкажіть формулу сульфатної (сірчаної) кислоти |
| 1 | Н2SО4 | 17, 18, 19 |
| 2 | S(ОН)3 | 4 |
| 3 | Н2SО3 | 4 |
| • 15 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Які з наведених кислот не реагують з міддю? |
| 1 | Н2SО4 (конц.) | 4 |
| 2 | НNО3 | 4 |
| 3 | НСl | 17, 18, 19 |
| • 16 |
| Ограничение времени | 5 минут |
| Текст к ситуации | Яким буде продукт відновлення концентрованої сірчаної (сульфатної) кислоти при взаємодії з цинком? |
| 1 | SО3 | 4 |
| 2 | SО2 | 4 |
| 3 | Н2S | 17 |
| • 17 |
| Текст к ситуации | Ви успішно завершили тестування.
Можна приступити до виконання лабораторної роботи № 1 "КЛАСИ НЕОРГАНІЧНИХ СПОЛУК" |
| 1 | Продовжити виконання лабораторної роботи | 18 |
| • 18 |
| Текст к ситуации | Лабораторнаробота № 1
"Класи неорганічних сполук" Перед виконанням дослідів ознайомтесь з формою звіту, який Ви маєте за-повнити під час лабораторної роботи після виконання кожного досліду (або після виконання всієї роботи), та надіслати викладачу. В першому досліді звіта подано зразок оформлення лабораторної роботи!
МІНІСТЕРСТВО ОСВІТИ УКРАЇНИ ХМЕЛЬНИЦЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ Кафедра хімії З В І ТВИКОНАННЯЛАБОРОТОРНОЇ РОБОТИ № 1 "КЛАСИ НЕОРГАНІЧНИХ СПОЛУК" Виконав: Студент_____________________________ Група___________________ Дослід 1. Одержання сульфур(ІV) оксиду та дослідження його властивостей.
Дослід 2.Одержання магній оксиду та дослідження його властивостей.
Дослід 3а. Одержання нікол гідроксиду, вивчення його властивостей.
Дослід 3б. Одержання цинк гідроксиду, вивчення його властивостей.
Дослід 3в. Одержання хром(ІІІ) гідроксиду, вивчення його властивостей.
Дослід 4а,Вивчення властивостей кислот. Взаємодія цинку з розчином хлоридної кислоти.
Дослід 4б,Вивчення властивостей кислот. Взаємодія міді з розчином сульфатної кислоти.
Дослід 4в,Вивчення властивостей кислот. Взаємодія міді з концентрованою сульфатною кислотою.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 20 |
| • 19 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 20 |
| • 20 |
| Иллюстрация к шагу | 0194-01-020.mp4 |
| Текст к ситуации | Дослід 1. Одержання сульфур(ІV) оксиду та дослідження його властивостей
Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 21 |
| • 21 |
| Иллюстрация к шагу | 0194-01-021-00.jpg |
| Текст к ситуации | Схема досліду 1.
В колбу наливаємо невелику кількість води, додаємо декілька краплин натрій гідроксиду та фенолфталеїну. В ложці для спалювання запалюємо сірку і вносимо в колбу, збираємо в колбі газ, збовтуємо. Як змінюється забарвлення фенолфталеїну при розчиненні SО2 у воді? |
| 1 | Рожевий → Безбарвний | 22 |
| 2 | Безбарвний → Рожевий | 19 |
| 3 | Жовтий → Рожевий | 19 |
| • 22 |
| Текст к ситуации | Напишіть реакцію взаємодії SО2 з водою |
| 1 | SО2 + Н2О = Н2SО3 | 23 |
| 2 | SО2 + Н2О = Н2SО4 | 19 |
| 3 | SО2 + Н2О = Н2SО2 | 19 |
| • 23 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 1.
Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи. Далі можна приступити до виконання Досліду 2.
Дослід 1. Одержання сульфур(ІV) оксиду та дослідження його властивостей.
| |||||||||||||||||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 25 |
| • 24 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 25 |
| • 25 |
| Иллюстрация к шагу | 0194-01-025.mp4 |
| Текст к ситуации | Дослід 2. Одержання магній оксиду та дослідження його властивостей
Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 26 |
| • 26 |
| Иллюстрация к шагу | 0194-01-026-00.jpg |
| Текст к ситуации | Схема досліду 2.
У чистий залізній ложечці спалюємо декілька шматочків стружок магнію. Продукт реакції розчиняємо у воді, додаємо краплю фенолфталеїну, а потім приливаємо розчин хлоридної кислоти. Якого кольору набуває розчин фенолфталеїну в присутності магній гідроксиду? |
| 1 | Безбарвний | 24 |
| 2 | Рожевий | 27 |
| 3 | Жовтий | 24 |
| • 27 |
| Текст к ситуации | Напишіть рівняння реакції магній оксиду з водою |
| 1 | Мg2О + Н2О = 2МgОН | 24 |
| 2 | МgО + Н2О = Мg(ОН)2 | 28 |
| 3 | Мg2О3 + 3Н2О = 2Мg(ОН)3 | 24 |
| • 28 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 2.
Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи. Далі можна приступити до виконання Досліду 3а.
Дослід 2.Одержання магній оксиду та дослідження його властивостей.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 30 |
| • 29 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 30 |
| • 30 |
| Иллюстрация к шагу | 0194-01-030.mp4 |
| Текст к ситуации | Дослід 3а. Одержання нікол(ІІ) гідроксиду, вивчення його властивостей
Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 31 |
| • 31 |
| Иллюстрация к шагу | 0194-01-031-00.jpg |
| Текст к ситуации | Схема досліду 3а.
Взаємодією розчину нікол сульфату з лугом одержуємо нерозчинний гідроксид ніколу. Розділимо осад на дві пробірки і досліджуємо відношення гідроксиду до дії кислоти і лугу. Який колір має осад нікол(ІІ) гідроксиду? |
| 1 | Рожевий | 29 |
| 2 | Синій | 29 |
| 3 | Зелений | 32 |
| • 32 |
| Текст к ситуации | Напишіть рівняння реакції нікол(ІІ) гідроксиду з хлоридною кислотою |
| 1 | Nі(ОН)2 + 2НСl = NіСl2 + 2Н2О | 33 |
| 2 | Nі(ОН)2 + 2НСlО4 = Nі(СlО4)2 + 2Н2О | 29 |
| 3 | Nі(ОН)3 + 3НСl = NіСl3 + 3Н2О | 29 |
| • 33 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 3а.
Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи. Далі можна приступити до виконання Досліду 3б.
Дослід 3а. Одержання нікол гідроксиду, вивчення його властивостей.
| ||||||||||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 35 |
| • 34 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 35 |
| • 35 |
| Иллюстрация к шагу | 0194-01-035.mp4 |
| Текст к ситуации | Дослід 3б. Одержання цинк гідроксиду, вивчення його властивостей
Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 36 |
| • 36 |
| Иллюстрация к шагу | 0194-01-036-00.jpg |
| Текст к ситуации | Схема досліду 3б.
Взаємодією розчину цинк сульфату з лугом одержуємо нерозчинний гідроксид цинку Розділимо осад на дві пробірки і досліджуємо відношення гідроксиду до дії кислоти і лугу. Якого кольору осад утворюється при взаємодії розчинів цинк сульфату та натрій гідроксиду? |
| 1 | Зеленкуватий | 34 |
| 2 | Блакитний | 34 |
| 3 | Білий | 37 |
| • 37 |
| Текст к ситуации | Виберіть реакції, характерні для цинк гідроксиду |
| 1 | Тільки Zn(ОН)2 + 2НСl = ZnСl2 + 2Н2О | 34 |
| 2 | Zn(ОН)2 + 2НСl = ZnСl2 + 2Н2О; Zn(ОН)2 + 2NаОН = Nа2[Zn(ОН)4] | 38 |
| 3 | Тільки Zn(ОН)2 + 2NаОН = Nа2[Zn(ОН)4] | 34 |
| • 38 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 3б.
Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи. Далі можна приступити до виконання Досліду 3в.
Дослід 3б. Одержання цинк гідроксиду, вивчення його властивостей.
| ||||||||||||||||||||||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 40 |
| • 39 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 40 |
| • 40 |
| Иллюстрация к шагу | 0194-01-040.mp4 |
| Текст к ситуации | Дослід 3в. Одержання хром(ІІІ) гідроксиду, вивчення його властивостей
Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 41 |
| • 41 |
| Иллюстрация к шагу | 0194-01-041-00.jpg |
| Текст к ситуации | Схема досліду 3в.
Взаємодією розчину хром(ІІІ) сульфату з лугом одержуємо нерозчинний гідроксид хрому. Розділимо осад на дві пробірки і досліджуємо відношення гідроксиду до дії кислоти і лугу. Якого кольору осад утворюється при взаємодії розчинів хром(ІІІ) сульфату та натрій гідроксиду? |
| 1 | Синій | 39 |
| 2 | Сіро-зелений | 42 |
| 3 | Блакитний | 39 |
| • 42 |
| Текст к ситуации | Виберіть реакції, характерні для хром(ІІІ) гідроксиду |
| 1 | Тільки Сr(ОН)3 + 3НСl = СrСl3 + 3Н2О | 39 |
| 2 | Сr(ОН)3 + 3НСl = СrСl3 + 3Н2О; Сr(ОН)3 + 3NаОН = Nа3[Zn(ОН)6] | 43 |
| 3 | Тільки Сr(ОН)3 + 3NаОН = Nа3[Zn(ОН)6] | 39 |
| • 43 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 3в.
Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи. Далі можна приступити до виконання Досліду 4а.
Дослід 3в. Одержання хром(ІІІ) гідроксиду, вивчення його властивостей.
| ||||||||||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 45 |
| • 44 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 45 |
| • 45 |
| Иллюстрация к шагу | 0194-01-045.mp4 |
| Текст к ситуации | Вивчення властивостей кислот Дослід 4а. Взаємодія цинку з хлоридною кислотою Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 46 |
| • 46 |
| Иллюстрация к шагу | 0194-01-046-00.jpg |
| Текст к ситуации | Схема досліду 4а.
Проводимо реакцію взаємодії цинку з розчином хлоридної кислоти. Який газ виділяється при взаємодії цинку з хлоридною кислотою? |
| 1 | Хлор | 44 |
| 2 | Водень | 47 |
| 3 | Кисень | 44 |
| • 47 |
| Текст к ситуации | Напишіть рівняння реакції взаємодії цинку з хлоридною кислотою |
| 1 | Zn + 2НСlО4 = Zn(СlО4)2 + Н2↑ | 44 |
| 2 | Zn + 2НСl = ZnСl2 + Н2↑ | 48 |
| 3 | Zn + НСl = ZnНСl | 44 |
| • 48 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 4а.
Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи. Далі можна приступити до виконання Досліду 4б.
Дослід 4а,Вивчення властивостей кислот. Взаємодія цинку з розчином хлоридної кислоти.
| ||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 50 |
| • 49 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 50 |
| • 50 |
| Иллюстрация к шагу | 0194-01-050.mp4 |
| Текст к ситуации | Вивчення властивостей кислот Дослід 4б. Взаємодія (?) міді з розведеною сульфатною кислотою Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 51 |
| • 51 |
| Иллюстрация к шагу | 0194-01-051-00.jpg |
| Текст к ситуации | Схема досліду 4б.
До мідних стружок додаємо розчин сульфатної кислоти. Чи реагує мідь з розведеною сульфатною кислотою? |
| 1 | Реагує з виділенням водню | 49 |
| 2 | Не реагує | 52 |
| 3 | Реагує з виділенням газу SО2 | 49 |
| • 52 |
| Текст к ситуации | Виберіть варіант, який відповідає вашим спостереженням |
| 1 | Реакція відбувається за рівнянням Сu + Н2SО4 = СuSО4 + Н2↑ | 49 |
| 2 | Реакція не відбувається | 53 |
| 3 | Реакція відбувається за рівнянням Сu + Н2SО4 = СuSО4 + SО2↑ + Н2О | 49 |
| • 53 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 4б.
Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи.
Далі можна приступити до виконання Досліду 4в.
Дослід 4б,Вивчення властивостей кислот. Взаємодія міді з розчином сульфатної кислоти.
| ||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 55 |
| • 54 |
| Текст к ситуации | Помилка тесту виконання лабораторної роботи.
На жаль, Ви обрали неправильний варіант відповіді. Вам необхідно повторити цей дослід лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 55 |
| • 55 |
| Иллюстрация к шагу | 0194-01-055.mp4 |
| Текст к ситуации | Вивчення властивостей кислот Дослід 4в. Взаємодія міді з концентрованою сульфатною кислотою Уважно продивіться відеофрагмент виконання досліду та його схему, дайте відповідь на наступні питання, занесіть результати спостереження та рівняння реакції у звіт виконання лабораторної роботи. |
| 1 | Продовжити виконання лабораторної роботи | 56 |
| • 56 |
| Иллюстрация к шагу | 0194-01-056-00.jpg |
| Текст к ситуации | Схема досліду 4в.
До мідних стружок додаємо концентровану сульфатну кислоту. Який запах має газ, що виділяється при взаємодії міді з концентрованою сульфатною кислотою? |
| 1 | Запах тухлих яєць | 54 |
| 2 | Немає запаху | 54 |
| 3 | Запах палених сірників | 57 |
| • 57 |
| Текст к ситуации | Напишіть рівняння реакції взаємодії міді з концентрованою сульфатною кислотою |
| 1 | Сu + Н2SО4 = СuSО4 + Н2 | 54 |
| 2 | Сu + 2Н2SО4 = СuSО4 + SО2 + 2Н2О | 58 |
| 3 | 2Сu + 3Н2SО3 = 2СuSО3 + S + 3Н2О | 54 |
| • 58 |
| Текст к ситуации | Ви успішно завершили виконання Досдіду 4в. Занесіть результати спостереження та рівняння реакцій в протокол виконання лабораторної роботи. Далі можна приступити до завершення заповнення протоколу виконання лабораторної роботи. Дослід 4в, Вивчення властивостей кислот. Взаємодія міді з концентрованою сульфатною кислотою.
| ||||||||||||||||||||
| 1 | Продовжити виконання лабораторної роботи | 59 |
| • 59 |
| Текст к ситуации | ВІТАЄМО ВАС!Ви успішно закінчили лабораторну роботу № 1 Перевірте правильність заповнення протоколу виконання лабораторної роботи № 1 та надішліть його викладачу для перевірки (на адресу деканату заочного дистанційного навчання) |