Лабораторна робота № 2
"ОКИСНО-ВІДНОВНІ РЕАКЦІЇ"
Звіт лабораторної роботи заповнюється у формі таблиці після виконання лабораторної роботи або після виконання кожного досліду. Ми рекомендуємо заповняти таблицю звіту після виконання кожного досліду! Ознайомтесь з повною формою оформлення звіту. На прикладі першого досліду подано зразок оформлення лабораторних дослідів.
Починайте виконувати досліди. Бажаємо успіху!
МІНІСТЕРСТВО ОСВІТИ УКРАЇНИ
ХМЕЛЬНИЦЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ
Кафедра хімії
З В І Т
ВИКОНАННЯ
ЛабораторнОЇ роботИ № 2
"ОКИСНО-ВІДНОВНІ ПРОЦЕСИ"
Виконав:
Студент_____________________________
Група___________________
Дослід 1. Відновлювальні властивості металів.
а) 3 Сu + 8 НNО3 (РОЗВЕД.) = 3 Сu(NО3)2 + 2 NО + 4 Н2О | ||||
| Мідь, Червонуваті ошурки | Нітратна кислота, Безбарвний розчин | Купрум(ІІ) нітрат, Блакитний розчин | Нітроген(ІІ) оксид, безбарвний газ | (Назва, 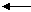 опис) опис) |
| Електронний баланс:
| ||||
Спостереження: Утворюється розчин блакитного кольору – купрум(ІІ) сульфату, | ||||
б) СuSО4 (РОЗЧИН) + Zn= … + … | |||
Електронний | |||
Спостереження:
| |||
Висновок: метали у вільному стані в окисно-відновних реакціях можуть проявляти властивості (окисників, відновників – підкреслити) | |||
Дослід 2. Окиснювальні властивості калій перманганату в різних середовищах.
а) КМnО4 + Nа2SО3 + Н2SО4 = МnSО4 + Nа2SО4 + К2SО4 + Н2О | |||
Електронний | |||
Спостереження:
| |||
б) КМnО4 + Nа2SО3 + Н2О= МnО2 + Nа2SО4 + КОН | |||
Електронний | |||
Спостереження: | |||
в) КМnО4 + Nа2SО3 + КОН= К2МnО4 + Nа2SО4 + Н2О | |||
Електронний | |||
Спостереження: | |||
Висновок:
| |||
Дослід 3. Окисно-відновна двоїстність.
а) КМnО4 + NаNО2 + Н2SО4 = МnSО4 + NаNО3 + К2SО4 + Н2О | |||
Електронний | |||
Спостереження:
| |||
б) КІ+ NаNО2 + Н2SО4 = І2 + NО + К2SО4 + Nа2SО4 | ||||
Електронний | ||||
Спостереження:
| ||||
Висновок: натрій нітрит виявляє властивості: в реакції (а) – ________________ в реакції (б) – ________________ | ||||
Дослід 4. Реакції внутрішньомолекулярного окиснення – відновлення.
(NН4)2Сr2О7 = N2 + Сr2О3 + Н2О | ||
Електронний | ||
Спостереження:
| ||
Висновок: амоній дихромат може вступати в реакцію внутрішньомолеку-лярного окиснення – відновлення тому, що _____________________________ ________________________________________________________ | ||